22. (6分)某市场销售的食用精制盐包装袋上有如下说明:
(6分)某市场销售的食用精制盐包装袋上有如下说明:
|
产品标准 |
GB5461 |
|
产品等级 |
一级 |
|
配
料 |
食盐、碘酸钾、抗结剂 |
|
碘含量(以I计) |
20~50mg/kg |
已知碘酸钾与碘化钾在酸性条件下发生如下反应:
 KIO3+5KI+3H2SO4 = 3K2SO4+3I2+3H2O。
KIO3+5KI+3H2SO4 = 3K2SO4+3I2+3H2O。
 (1)上述反应生成的I2可用四氯化碳萃取。向碘的四氯化碳溶液中加入Na2SO3稀溶液,
(1)上述反应生成的I2可用四氯化碳萃取。向碘的四氯化碳溶液中加入Na2SO3稀溶液,
 将I2还原(反应的离子方程式是I2+SO32-+H2O =
),以回收
将I2还原(反应的离子方程式是I2+SO32-+H2O =
),以回收
 四氯化碳。某学生设计回收四氯化碳的操作步骤为:
四氯化碳。某学生设计回收四氯化碳的操作步骤为:
 a.将碘的四氯化碳溶液置于分液漏斗中
a.将碘的四氯化碳溶液置于分液漏斗中
 b.加入适量Na2SO3稀溶液
b.加入适量Na2SO3稀溶液
 c.分离出
(填“上”或“下”)层液体加以回收
c.分离出
(填“上”或“下”)层液体加以回收
 以上设计中有遗漏,在操作步骤b后,应增加的操作为:
。
以上设计中有遗漏,在操作步骤b后,应增加的操作为:
。
 (2)已知:I2+2S2O32-(无色)=2I-+S4O62-(无色)。某学生测定食用精制盐的碘含量,其
(2)已知:I2+2S2O32-(无色)=2I-+S4O62-(无色)。某学生测定食用精制盐的碘含量,其
 步骤为:
步骤为:
 a.准确称取w g食盐,加适量蒸馏水使其完全溶解
a.准确称取w g食盐,加适量蒸馏水使其完全溶解
 b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与之反应完全
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与之反应完全
 c.以 为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3
c.以 为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3
 溶液10.0ml,此时溶液恰好由
色变为 色。
溶液10.0ml,此时溶液恰好由
色变为 色。

21. (4分)为了检验和除去下表中的各种所含杂质(括号里的物质),请从(Ⅰ)中选出
(4分)为了检验和除去下表中的各种所含杂质(括号里的物质),请从(Ⅰ)中选出
 适当的检验试剂,从(Ⅱ)中选出适当的除杂试剂,将所选的答案填入相应的空格内。
适当的检验试剂,从(Ⅱ)中选出适当的除杂试剂,将所选的答案填入相应的空格内。
|
物质 |
检验试剂 |
除杂试剂 |
|
甲烷(乙烯) |
|
|
|
酒精(水) |
|
|
(Ⅰ)检验的试剂:A.无水硫酸铜 B.酸性高锰酸钾溶液
 C.盐酸 D.氢氧化钠溶液
C.盐酸 D.氢氧化钠溶液
 (Ⅱ)除杂试剂: a.硫酸 b.乙酸
c.新制的生石灰 d.溴水
(Ⅱ)除杂试剂: a.硫酸 b.乙酸
c.新制的生石灰 d.溴水
20. 将气体甲通入液体乙中得一混合液,取一定质量的该
将气体甲通入液体乙中得一混合液,取一定质量的该

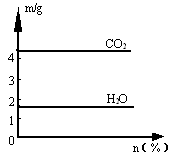 混合液进行完全燃烧实验,生成CO2、H2O的质量与甲
混合液进行完全燃烧实验,生成CO2、H2O的质量与甲
 气体在混合液中质量分数关系如右图所示,甲、乙组合
气体在混合液中质量分数关系如右图所示,甲、乙组合
 正确的是
正确的是
|
|
A |
B |
C |
D |
|
甲 |
乙烯 |
甲烷 |
乙炔(C2H2) |
乙烷 |
|
乙 |
环己烷(C6H12) |
苯 |
苯 |
乙醇 |





19. 根据事实所作结论,正确的是
根据事实所作结论,正确的是
|
编号 |
事实 |
结论 |
|
A |
某溶液中滴加BaCl2溶液,生成不溶于稀HNO3的白色沉淀 |
该溶液中一定含有SO42- |
|
B |
某固体中加入NaOH溶液,产生了使湿润红色石蕊试纸变蓝的气体 |
该固体中一定含有NH4+ |
|
C |
在淀粉溶液中加入淀粉酶,一段时间后取出部分水解液,滴加碘水,不变蓝 |
水解液中已经不含有高分子化合物 |
|
D |
邻二甲苯只有一种结构 |
苯分子中碳碳键完全相同,而不是单双键交替结构 |
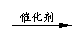 ②用甲烷、一氧化碳合成乙酸乙酯:2CH4+2CO
CH3COOC2H5
②用甲烷、一氧化碳合成乙酸乙酯:2CH4+2CO
CH3COOC2H5