21. 小远通过查阅资料知道了牙膏的主要成分。他将一定比例的碳酸钙粉末和食盐倒入小烧杯中,然后加入适量甘油(保湿剂)、甜味剂和香精等,搅拌均匀后制得牙膏。
(1)牙膏是___________________ (填“纯净物”和“混合物”)
(2)小远测定自制牙膏及其他清洁用品的pH,记录如下:
|
物质 |
自制牙膏 |
洁厕灵 |
油污净 |
|
pH |
S |
2 |
12 |
自制牙膏显___________(填“酸性”、“碱性”或“中性”),洁厕灵可使紫色石蕊试液变_____。
(3)牙膏中的碳酸钙粉末作摩擦剂,提高洁齿效果。这种碳酸钙是将二氧化碳通入石灰浆制得的。请写出以石灰石和水为原料制取这种碳酸钙的化学方程式。
__________________________________________________________________________
20. 六朝古都南京的一些古代建筑保存完好,这与所用的建筑材料有关。该小组从某古代建筑维修现场搜集了一些旧墙灰进行研究。取12.0g旧墙灰(主要成分是碳酸钙)放入烧杯中,并加入足量稀盐酸(假设其他也杂质不参加反应,不考虑H2O、HCl逸出)。反应开始时,烧杯及所盛物质的总质量为300.0g。实验数据记录如下:
|
反应时间/min |
0 |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
16 |
18 |
|
烧杯及所盛物 质总质量/g |
300.0 |
299.0 |
298.0 |
297.2 |
296.5 |
296.0 |
295.7 |
295.6 |
M |
295.6 |
 (1)该小组因故没有记录反应时间为16min时的数据M。你由表中数据推测,M=______g;
(1)该小组因故没有记录反应时间为16min时的数据M。你由表中数据推测,M=______g;
(2)反应生成CO2的总质量为_____________g;
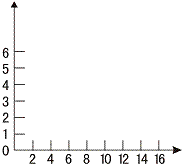
(3)根据实验数据,在右边的坐标纸上绘制生成
CO2质量与反应时间关系的曲线。前3min生成
CO2的质量为___________g;
(4)该旧墙灰中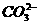 离子的质量分数为______。
离子的质量分数为______。
18. 钛(Ti)因为具有许多神奇的性能而越来越引起人们的关注。某化学兴趣小组对Mg、Ti、Ag的金属活动性顺序进行探究。提出假设:a.Ti的金属活动性比Mg 强; b.Ti的金属活动性介于Mg和Ag之间。
查阅资料:在相同条件下,金属与酸反应,产生气泡的速度越快,则该金属活动性越强。
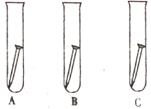
实验设计:同温下,取大小相同的这三种金属薄片,分别投入等体积、等质量分数的足量稀盐酸中,观察现象。
(1)三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是_______(填序号)。
①除去氧化膜,利于直接反应 ②使反应的金属温度相同,易反应 ③使表面光亮,易观察现象
|
金属 |
Ti |
Mg |
Ab |
|
实验现象 |
产生气泡速度缓慢 |
产生气泡速度快 |
无任何现象 |
(2)根据下表中的实验现象填空:
结论:原假设中__________不正确(填“a”、“b”或“ab”),理由是___________;三种金属的活动性由强到弱的顺序为______________________________。
(3)上述实验设计中,如果所用盐酸的溶质质量分数不同,是否一定能够得出正确的结论?________(填“是”或“否”),理由是______________。
 全世界每年因生锈而损失的钢铁,约占世界钢铁年产量的
全世界每年因生锈而损失的钢铁,约占世界钢铁年产量的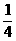 ,某同
,某同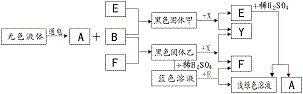 右图为一些常见物质间互相转化的关系图(有些反应条件已省略):已知高温下CO能与多种金属氧化物反应生成相应的金属和CO2。下列关系图中,A、B、X、Y均为无色气体,E、F为常见金属。
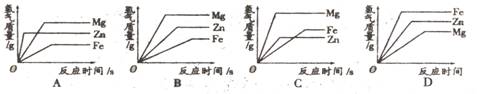
右图为一些常见物质间互相转化的关系图(有些反应条件已省略):已知高温下CO能与多种金属氧化物反应生成相应的金属和CO2。下列关系图中,A、B、X、Y均为无色气体,E、F为常见金属。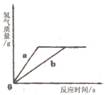 用质量相等的锌粉和铁粉,分别与溶质质量分数相同、等质量的稀盐酸充分反应,产生氢气的质量和反应所用时间的关系如上图所示。则下列说法不正确的是 ( )
用质量相等的锌粉和铁粉,分别与溶质质量分数相同、等质量的稀盐酸充分反应,产生氢气的质量和反应所用时间的关系如上图所示。则下列说法不正确的是 ( )