2.实验中收集到的氧气总是含有一些杂质气体,那么怎样收集到比较纯净的氧气?
剖析:如果要收集到比较纯净的气体,就要注意避免空气的干扰。首先使用排水法收集时,集气瓶中要灌满水,将瓶内的空气彻底排尽,然后再收集时,要等到有连续均匀的气泡产生时再收集,最后取出集气瓶时要在水下盖好集气瓶,正放到桌面上。排空气法收集到的氧气总是多多少少含有空气的,所以要把导气管放到集气瓶底部,利用氧气的密度比空气大的性质把空气向上排出。
问题探究
问题 小明同学通过查阅有关资料,想通过下面两图所示仪器、药品、装置进行实验探究:寻找新的催化剂--氧化铁能作过氧化氢分解的催化剂吗?过程如下:
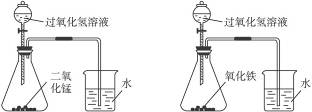
图3-4
猜想:氧化铁粉末能作过氧化氢分解的催化剂,能加快过氧化氢分解放出氧气的速率。
实验探究:按如上图所示装置进行实验,实验步骤及现象为:
(1)在两个锥形瓶中分别装入等质量的二氧化锰和氧化铁,通过分液漏斗同时以相同速率逐滴滴入过氧化氢溶液。观察到通入水中的导管均有气泡冒出,且加二氧化锰的导管口放出气泡的速率更快。
(2)实验后把二氧化锰和氧化铁分别洗净、干燥,再称量,发现氧化铁和二氧化锰在反应前后的质量都没有变化。
结论:氧化铁可作过氧化氢分解的催化剂,但比二氧化锰催化作用要弱些。
典题精讲
例1实验室常用高锰酸钾和二氧化锰制取氧气(见图3-5装置A),也可用过氧化氢和催化剂二氧化锰来制取氧气(见图3-5装置B)。装置B中的仪器a是分液漏斗,通过活塞的“开”“关”可以随时滴加过氧化氢溶液,从而控制得到氧气的量。
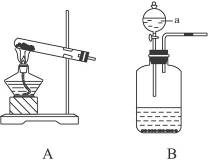
图3-5
(1)从反应物状态和反应条件来比较装置A和B的差异:
|
|
装置A |
装置B |
|
反应状态 |
|
|
|
反应条件 |
|
|
(2)用装置B制得的氧气带有少量水蒸气,可用浓硫酸除去水蒸气,请在下列方框中添上带橡皮塞的玻璃导管,完成除去水蒸气的装置图(见图3-6)。
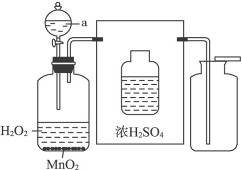
图3-6
(3)用向上排空气法收集氧气,并用带火星的木条放在集气瓶口检验氧气是否收集满,这是利用了氧气的_______、_______性质。
思路解析 先要明确装置A适合固体药品和固体药品反应进行实验并且可以加热,高锰酸钾为固体,反应条件为加热;装置B是用过氧化氢和催化剂二氧化锰粉末来制取氧气,其中反应物过氧化氢为液体,反应条件为不需加热。当用浓硫酸来除去水蒸气时,为了有利于水蒸气的充分吸收,进入瓶中的导气管要插入液体中。氧气之所以能用向上排空气法收集是因为它的密度比空气大,并且因为它具助燃性,所以能使带火星的木条复燃。
答案:(1)反应物为固体 反应物为液体 需加热 不需加热
(2)
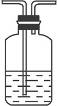
图3-9
(3)密度比空气大 助燃性
例2如图所示的装置中,其中收集氧气时可选用( )
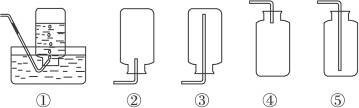
图3-10
A.①和② B.②和③ C.①和④ D.①和⑤
思路解析 根据氧气不易溶于水,且不与水反应,可用排水法收集;在通常情况下,氧气密度比空气密度略大,且不与空气中的任何其他成分反应,可用向上排空气法收集,收集时,导管口应接近集气瓶瓶底,便于将集气瓶内的空气排尽。
答案:D
例3某学生在做实验室制氧气实验时,采用图3-12所示装置,实验结束后,发现试管炸裂,试分析造成此后果的可能原因。

图3-12
思路解析 该实验采用的是在试管中加热固体物质产生气体,并用排水法收集气体的一套组合装置,因而分析试管破裂的原因应从酒精灯的正确使用、固体物质的加热方法、排水集气法收集气体等方面进行分析。
答案:给试管加热时,试管外壁有水珠没擦干就加热或没预热,直接加热盛药品部位,使试管局部骤热;受高温的试管底部碰着了酒精灯的灯芯;实验结束时,先撤去酒精灯,再使导管移出水槽,致使水倒流进试管。以上错误操作都有可能导致试管炸裂。
知识导学
本节课同学们要在探究活动中学习掌握实验室制氧气的药品、反应原理、仪器装置、收集气体的方法、验满及注意事项,同时认识催化剂及其作用。
实验探究是本节课学习的主要方法。在做实验中要形成观察实验现象→分析原因→得出结论的探究能力。在众多方案中通过对比我们可以发现简便易行、经济无污染的方案是实验室制氧气的最佳方案。
氧气的制法有多种,例如:①电解水可以制得氧气;②加热高锰酸钾或氯酸钾可以制得氧气;③用过氧化氢溶液为原料,以二氧化锰作催化剂也可以制得氧气。我们可以通过实验探究,运用对比的方法从众多的实验方案中选择最佳方案。当然你也可以自己设计实验方案,对于不正确或可能不成功的方案,只要没有危险,在老师的同意下你可以试一试,从探索中体验到成功的乐趣或获得失败的教训,你一定会有很大收获的。
收集方法从氧气的密度和溶解性来考虑。密度比空气大,不溶于水,两种方法都可用,但平时我们主要用排水法收集,这是因为排水法收集的氧气比较纯净,而由于氧气的密度与空气的密度比较接近,排空气时,很难排净空气,这样收集的氧气纯度不高。
鉴别氧气根据氧气的化学性质支持燃烧,能使带火星的木条复燃。
在理解催化剂的概念时,应注意以下几点:(1)它能改变(加快或减慢)其他物质的化学反应速率,不能片面地说加快;(2)二氧化锰并不是专作催化剂用的,如用高锰酸钾制氧气时是生成物,在某些反应中作为反应物;(3)二氧化锰对双氧水的分解具有催化作用,但不是唯一的,如沸石、生土豆也对双氧水的分解具有催化作用;(4)催化剂只能改变化学反应速率,不能增大或减少生成物的质量。
疑难导析
该问题考查的是催化剂的概念。学习时要抓住催化剂特点:“一变两不变”,一变指催化剂能改变其他物质的化学反应速率;两不变是指反应前后催化剂的质量和化学性质不变。
要清楚用排水法收集氧气时,刚开始从导管口排出的是试管里受热膨胀的空气,由此说明开始放出的气泡能否收集,在什么时候再将导管伸入盛满水的集气瓶口收集,当集气瓶口边缘出现什么现象时,表明集气瓶内水已排完,气体收集满了,此时,收集满的气体应如何放置。用向上排空气法收集时,导管应接近集气瓶的什么位置,这样操作的目的是什么,在集气瓶口盖上一块硬纸片的目的是什么。
问题导思
这是研究性学习问题的范例,以问题情景为课题,积极探究,自主发现,实验探究,合作交流。通过比较反应的速率寻找新的催化剂。
探究本问题首先要理解催化剂的概念,要抓住催化剂特点:“一变两不变”。 一是要设计实验探究催化剂能改变过氧化氢的分解速率;二是要设计实验探究催化剂的质量和化学性质都不变。
氧化铁能否作催化剂呢?可通过对比实验,比较过氧化氢分解产生氧气的速率作出判断,反应完后还要称一下氧化铁反应前后的质量,看有无变化。所以首先要取等质量的二氧化锰和氧化铁,然后分别和过氧化氢反应。通过观察放出气泡的速率来判断催化剂对反应速率的影响。在反应完成后,还要进行检验催化剂质量有无变化的物质分离和称量实验。
注意催化剂的分离,利用催化剂与其他物质的性质不同,可采用过滤,洗涤的方法,最后烘干再称量。
典题导考
绿色通道 搞清制取氧气的多种方法,根据反应物的状态和性质及反应条件而采用不同的反应装置。对于气体的净化装置,橡皮塞上的玻璃导管,进气管和出气管哪一根应该长,首先要弄清题目的要求,再判断从哪边进气。
典题变式
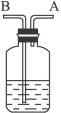
 水+氧气
催化作用 B
氧气密度比空气大 (2)A A
水+氧气
催化作用 B
氧气密度比空气大 (2)A A