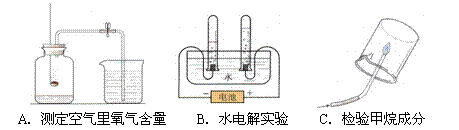
35.(3分)食用纯碱的主要成分是碳酸钠,另外还含有少量的氯化钠。为了测定某品牌食用纯碱中碳酸钠的质量分数,某校化学研究性学习小组的同学进行了如下实验:(反应过程中不考虑水和氯化氢的挥发。)
|
加入稀盐酸次数 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
烧杯及所称物质总质量/g |
78.90 |
97.80 |
116.70 |
135.60 |
155.05 |
175.05 |
195.05 |
取13.5g样品放入烧杯中,每次加入20g稀盐酸(不考虑水、氯化氢逸出)后用精密仪器称量,记录实验数据如下:(计算结果保留2位小数)
(1)计算样品中碳酸钠的质量分数
(2)计算实验时所用稀盐酸中溶质的质量分数。
33.(7分)请你参与某学习小组进行研究性学习的过程,并协助完成相关任务。
小华同学向一定量的纯碱溶液中投入一定量的生石灰,充分反应,冷却到常温后,观察 到有白色不溶物,过滤,得滤液A和白色固体B。
写出上述实验中有关的化学方程式:____________________________。
[问 题]滤液成分是什么?白色固体的成分是什么?
[猜 想]请补充完成下列猜想。
|
猜 想 |
⑴ |
⑵ |
⑶ |
⑷ |
|
滤液A中的溶质 |
NaOH |
NaOH Na2CO3 |
NaOH Ca(OH)2 |
|
|
白色固体B的成分 |
CaCO3 |
|
CaCO3 |
CaCO3 Ca(OH)2 |
[实 验]实验得知,猜想(4)是正确的。请完成下列实验报告,证明猜想(4)的白色固体B的成分。
|
实 验 步 骤 |
实 验 现 象 |
实 验 结 论 |
|
|
|
白色固体B中的成分是CaCO3、Ca(OH)2 |
[拓展与应用]实验完成后,小华欲从滤液A中得到纯净的氢氧化钠固体,于是找来小明和小聪设计了如下的实验方案:

但在选择试剂B上产生了分歧,小明认为应通入适量的二氧化碳气体,而小华、小聪认为应该加入过量的碳酸钠溶液,你认为他们选择的试剂是否能达到实验目的,并说明理由
。

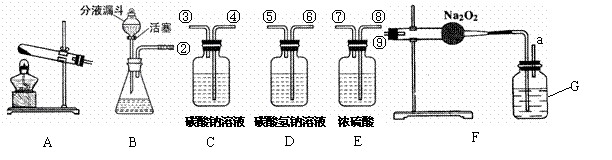
 (6分)根据图中所示装置回答问题:
(6分)根据图中所示装置回答问题: