26.(15分)装修材料中常用作红色颜料的有三氧化二铁和氧化亚铜。某学生想通过实验探究一红色粉末的成分。其探究过程如下:
查阅资料:Cu2O溶于稀硫酸生成Cu和CuSO4,在空气中缓慢加热生成CuO。
提出假设:
假设1:红色粉末是Fe2O3;
假设2:红色粉末是Cu2O;
假设3: 。
设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加KSCN试剂。
(1)若假设1成立,则实验现象是 。
(2)若固体粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红色,则证明原固体粉末是 。
(3)实验小组欲用加热法测定Cu2O的质量分数。取ag固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为
(4)实验小组欲利用含Fe2O3和Cu2O的红色粉末制取纯净的胆矾(CuSO4·5H2O)。经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
|
物质 |
Cu(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
|
开始沉淀pH |
6.0 |
7.5 |
1.4 |
|
沉淀完全pH |
13 |
14 |
3.7 |
实验室有下列试剂可供选择:A.氯水 B.H2O2 C.NaOH D.Cu(OH)2,实验小组设计如下实验方案:
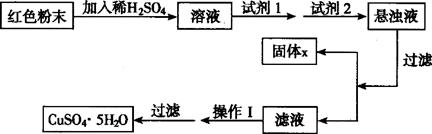
①试剂1为 ,试剂2为 (选填字母A、B、C、D)。
②固体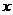 的化学式为
。
的化学式为
。
③操作Ⅰ-------- 。
25.(15分)A、B、C、D是原子序数依次增大的四种短周期元素。请根据表中信息回答下列问题。
|
元素 |
A |
B |
C |
D |
|
性质或结构 信息 |
与同主族元素原子序数相差2 |
原子的最外层电子排布式为nsnnp2n-1 |
原子序数是A、B两元素原子序数之和的2倍 |
原子半径在所属周期中最小 |
(1)写出B原子的最外层轨道排布式______________________。
(2) A与B的单质可化合生成M,A与D的单质可化合生成N,M的空间构型为_____________。M与N可以在空气中化合生成E,E的电子式为____________________,写出在E溶于水所得的溶液中各离子浓度由大到小的顺序________________________。
(3)C的单质在空气中燃烧可生成气体F,写出F与A、C形成的化合物反应的方程式,并标出电子转移的方向和数目 _ ,F与A、B、D单质中的一种在溶液中充分反应可生成两种酸,写出该反应的离子方程式 。
19.在足够大的匀强磁场中,静止的钠的同位素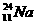 发生衰变,沿与磁场垂直的方向释放出一个粒子后,变为一个新核.新核与放出粒子在磁场中运动的径迹均为圆,如图所示。
发生衰变,沿与磁场垂直的方向释放出一个粒子后,变为一个新核.新核与放出粒子在磁场中运动的径迹均为圆,如图所示。

|
|
|
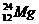
|

|
|
|
|
以上观点均正确的组合是( )
A.①③ B.②④ C.②③ D.①④
 光滑圆弧轨道,轨道上端切线水平。N为待检验的固定曲面,该曲面在竖直面内的截面为半径
光滑圆弧轨道,轨道上端切线水平。N为待检验的固定曲面,该曲面在竖直面内的截面为半径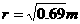 的
的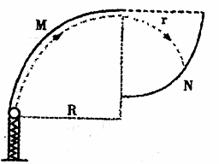
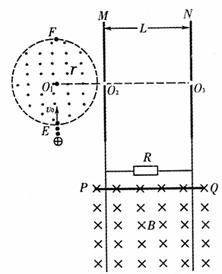 24.(22分)如图所示,半径为r、圆心为O1的虚线所围的圆形区域内存在垂直纸面向外的匀强磁场,在磁场右侧有一竖直放置的平行金属板M和N,两板间距离为L,在MN板中央各有一个小孔O2、O3、O1、O2、O3在同一水平直线上,与平行金属板相接的是两条竖直放置间距为L的足够长的光滑金属导轨,导体棒PQ与导轨接触良好,与阻值为R的电阻形成闭合回路(导轨与导体棒的电阻不计),该回路处在磁感应强度大小为B,方向垂直纸面向里的匀强磁场中,整个装置处在真空室中,有一束电荷量为+q、质量为m的粒子流(重力不计),以速率v0从圆形磁场边界上的最低点E沿半径方向射入圆形磁场区域,最后从小孔O3射出。现释放导体棒PQ,其下滑h后开始匀速运动,此后粒子恰好不能从O3射出,而从圆形磁场的最高点F射出。求:
24.(22分)如图所示,半径为r、圆心为O1的虚线所围的圆形区域内存在垂直纸面向外的匀强磁场,在磁场右侧有一竖直放置的平行金属板M和N,两板间距离为L,在MN板中央各有一个小孔O2、O3、O1、O2、O3在同一水平直线上,与平行金属板相接的是两条竖直放置间距为L的足够长的光滑金属导轨,导体棒PQ与导轨接触良好,与阻值为R的电阻形成闭合回路(导轨与导体棒的电阻不计),该回路处在磁感应强度大小为B,方向垂直纸面向里的匀强磁场中,整个装置处在真空室中,有一束电荷量为+q、质量为m的粒子流(重力不计),以速率v0从圆形磁场边界上的最低点E沿半径方向射入圆形磁场区域,最后从小孔O3射出。现释放导体棒PQ,其下滑h后开始匀速运动,此后粒子恰好不能从O3射出,而从圆形磁场的最高点F射出。求:
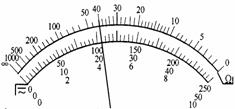 Ⅱ(10分)一额定功率为0.01W的电阻,其阻值不详。用欧姆表粗测其阻值结果如图所示(档位上×1K)。现有下列器材,试设计适当的电路,选择合适的器材,较精确地测定其阻值(滑动变阻器的调节要方便)。
Ⅱ(10分)一额定功率为0.01W的电阻,其阻值不详。用欧姆表粗测其阻值结果如图所示(档位上×1K)。现有下列器材,试设计适当的电路,选择合适的器材,较精确地测定其阻值(滑动变阻器的调节要方便)。 F.直流稳压电源,输出电压6V,额定电流3A
F.直流稳压电源,输出电压6V,额定电流3A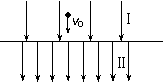 如图所示,在真空区域Ⅰ、Ⅱ中存在两个匀强电场,其电场线方向竖直向下,在区域Ⅰ中有一个带负电的粒子沿电场线以速度v0匀速下落,并进入区域Ⅱ(电场范围足够大)。能描述粒子在两个电场中运动的速度--时间图象是(以v0方向为正方向)( )
如图所示,在真空区域Ⅰ、Ⅱ中存在两个匀强电场,其电场线方向竖直向下,在区域Ⅰ中有一个带负电的粒子沿电场线以速度v0匀速下落,并进入区域Ⅱ(电场范围足够大)。能描述粒子在两个电场中运动的速度--时间图象是(以v0方向为正方向)( )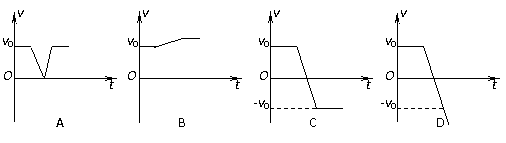


 如图所示,固定斜面倾角为θ,整个斜面分为AB、BC两段,且2AB=BC。小物块P(可视为质点)与AB、BC两段斜面之间的动摩擦因数分别为μ1、μ2。已知P由静止开始从A点释放,恰好能滑动到C点而停下,那么θ、μ1、μ2间应满足的关系是( )
如图所示,固定斜面倾角为θ,整个斜面分为AB、BC两段,且2AB=BC。小物块P(可视为质点)与AB、BC两段斜面之间的动摩擦因数分别为μ1、μ2。已知P由静止开始从A点释放,恰好能滑动到C点而停下,那么θ、μ1、μ2间应满足的关系是( )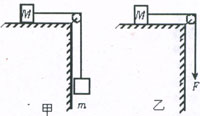 如图所示,甲图为光滑水平面上质量为M的物体,用细线通过定滑轮与质量为
如图所示,甲图为光滑水平面上质量为M的物体,用细线通过定滑轮与质量为 的物体相连,由静止释放;乙图为同一物体M在光滑水平面上用细线通过定滑轮竖直向下受到拉力
的物体相连,由静止释放;乙图为同一物体M在光滑水平面上用细线通过定滑轮竖直向下受到拉力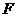 的作用(拉力
的作用(拉力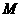 距桌边的距离相等,则( )
距桌边的距离相等,则( )