32.(18分)某课外小组对一些金属单质和化合物的性质进行研究。
下表为“铝与氯化铜溶液反应”实验报告的一部分:
|
实验步骤 |
实验现象 |
|
将打磨过的铝片(过量)放入一定 浓度的CuCl2溶液中 |
产生气泡,析出疏松的红色固体, 溶液逐渐变为无色 |
|
反应结束后分离出溶液备用 |
|
|
红色固体用蒸馏水洗涤后,置于 潮湿空气中 |
一段时间后固体由红色变为绿色 [视其主要成分为Cu2(OH)2CO3] |
(1)按反应类型写出实验中发生反应的化学方程式各一个(是离子反应的只写离子方程式)
置换反应_____________________________;化合反应______________________________。
(2)用石墨作电极,电解上述实验分离出的溶液,两极产生气泡。持续电解,在阴极附近的溶液中还可观察到的现象是_________________________________________。解释此现象的离子方程式是____________________________________________________________。
(3)工业上可用铝与钦锰矿(主要成分为MnO2)反应来冶炼金属锰。
①用铝与软锰矿冶炼锰的原理是(用化学方程式表示)______________________________。
②MnO2在H2O2分解反应中作催化剂。若将适量MnO2加入酸化后的H2O2溶液中,MnO2溶解产生Mn2+,该反应的离子方程式是______________________________________。
31.(12分)废旧印刷电路板的回收利用可实现资源再生,并减少污染。废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末。
(1)下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是 (填字母)。
A.热裂解形成燃油 B.露天焚烧
C.作为有机复合建筑材料的原料 D.直接填埋
(2)用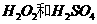 的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
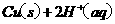 ====
====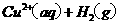
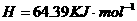
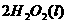 ====
====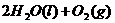
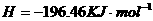
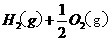 ====
====
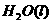
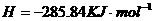
在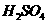 溶液中
溶液中 与
与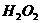 反应生成
反应生成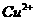 和
和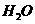 的热化学方程式为
。
的热化学方程式为
。
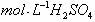 (3)控制其他条件相同,印刷电路板的金属粉末用10℅
(3)控制其他条件相同,印刷电路板的金属粉末用10℅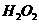 和3.0的混合溶液处理,测得不同温度下铜的平均溶解速率(见下表)。
和3.0的混合溶液处理,测得不同温度下铜的平均溶解速率(见下表)。
|
温度(℃) |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
|
铜平均溶解速率 ( 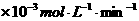 ) ) |
7.34 |
8.01 |
9.25 |
7.98 |
7.24 |
6.73 |
5.76 |
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是 。
(4)在提纯后的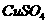 溶液中加入一定量的
溶液中加入一定量的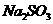 和
和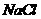 溶液,加热,生成
溶液,加热,生成 沉淀。制备
沉淀。制备 的离子方程式是
。
的离子方程式是
。
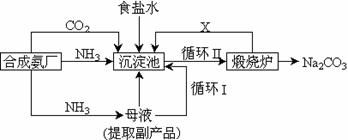
30.(18分)医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙(含有少量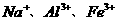 等杂志)生产医药级二水合氯化钙(
等杂志)生产医药级二水合氯化钙(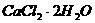 的质量分数为97.0%~103.0%)的主要流程如下:
的质量分数为97.0%~103.0%)的主要流程如下:
|
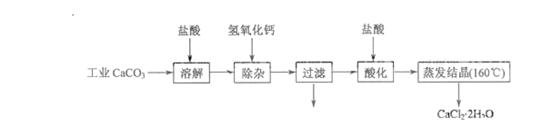
(1)除杂操作是加入氢氧化钙,调节溶液的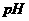 为8.0~8.5,以出去溶液中的少量
为8.0~8.5,以出去溶液中的少量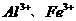 。检验
。检验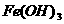 是否沉淀完全的试验操作是
。
是否沉淀完全的试验操作是
。
(2)酸化操作是加入盐酸,调节溶液的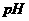 约为4.0,其目的有:①
; ②防止
约为4.0,其目的有:①
; ②防止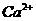 在蒸发时水解;③防止溶液吸收空气中CO2。
在蒸发时水解;③防止溶液吸收空气中CO2。
(3)测定样品中 含量的方法是:a.称取0.7500g样品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用0.05000
含量的方法是:a.称取0.7500g样品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用0.05000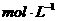
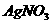 溶液滴定至终点,消耗
溶液滴定至终点,消耗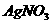 溶液体积的平均值为20.39mL。
溶液体积的平均值为20.39mL。
①上述测定过程中需要溶液润洗的仪器有 。
②计算上述样品中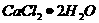 的质量分数为
。
的质量分数为
。
③若用上述办法测定的样品中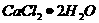 的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有
;
。
的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有
;
。
 处理细菌细胞膜改变其通透性,释放代谢产物以解除代谢产物对酶活性
处理细菌细胞膜改变其通透性,释放代谢产物以解除代谢产物对酶活性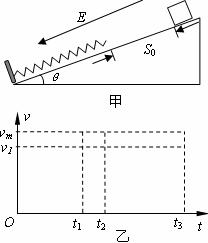 (3)从滑块静止释放瞬间开始计时,请在乙图中画出滑块在沿斜面向下运动的整个过程中速度与时间关系v-t图象。图中横坐标轴上的t1、t2及t3分别表示滑块第一次与弹簧上端接触、第一次速度达到最大值及第一次速度减为零的时刻,纵坐标轴上的v1为滑块在t1时刻的速度大小,vm是题中所指的物理量。(本小问不要求写出计算过程)
(3)从滑块静止释放瞬间开始计时,请在乙图中画出滑块在沿斜面向下运动的整个过程中速度与时间关系v-t图象。图中横坐标轴上的t1、t2及t3分别表示滑块第一次与弹簧上端接触、第一次速度达到最大值及第一次速度减为零的时刻,纵坐标轴上的v1为滑块在t1时刻的速度大小,vm是题中所指的物理量。(本小问不要求写出计算过程)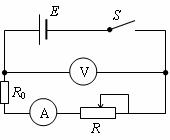 电流表(量程0.6A、3A);
电流表(量程0.6A、3A); 、额定功率5W)
、额定功率5W)