28.(18分) 某课外活动小组在实验室条件下探究CO与Fe2O3反应的情况,实验设计如图Ⅰ所示。
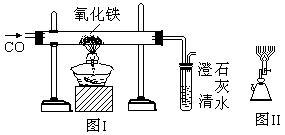
(1)上述装置中缺少尾气处理部分,如何进行尾气处理? 。
(2)当观察到固体粉末由红棕色完全变为黑色时,欲停止实验应进行的操作为
(3)然后,活动小组同学对所得黑色固体做了如下探究实验:
①用磁铁在玻璃管外壁感应,发现黑色固体感应移动。
②取少许黑色固体置于一支小试管中,加入稀盐酸,未见气体产生。
③另取少许黑色固体置于另一支小试管中,加入CuSO4溶液,振荡、静置,无明显现象。由此可判断该黑色固体成分 __ ___
a.肯定不含单质铁可能只含Fe3O4 b. 肯定含有单质铁
c. 可能是Fe3O4与FeO的混合物 d. 可能是FeO与Fe2O3的混合物
(4)于是,活动小组同学又取Fe2O3固体进行了定量实验,记录有关数据如下:
|
加热时间(min) |
0 |
4 |
8 |
12 |
16 |
|
固体质量(g) |
24.0 |
23.2 |
21.6 |
16.8 |
16.8 |
通过计算判断:加热到12min时所得固体产物为 (填化学式);若4 min时所得固体为纯净物,则在0-4min时间段里发生反应的化学方程式为 。
(5)又有同学把酒精灯换为酒精喷灯(如图Ⅱ,其火焰温度为700~800℃),仍取24.0g的Fe2O3粉末再次进行实验,加热了5 min时停止实验,冷却后称量,固体质量为16.8g由此得到启发,工业高炉炼铁在1000℃左右进行作业的原因是 。
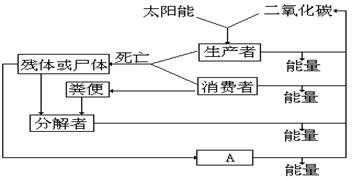
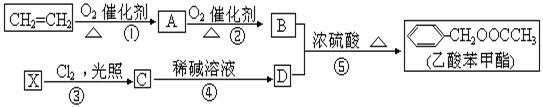
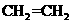 制得A(用类似以上流程图表示)
制得A(用类似以上流程图表示)
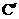 、
、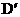 而得不到
而得不到 、
、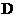 :
: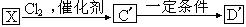
 溶液发生显色反应,写出符合条件的由X→
溶液发生显色反应,写出符合条件的由X→ (14分) 有M、A、B、D、E五种短周期元素,原子序数依次增大。M元素的单质是自然界最轻的气体。A、B、D、E分别在右表(周期表的一部分)不同的空格内占有相应的位置,它们的原子序数之和为37。试回答:
(14分) 有M、A、B、D、E五种短周期元素,原子序数依次增大。M元素的单质是自然界最轻的气体。A、B、D、E分别在右表(周期表的一部分)不同的空格内占有相应的位置,它们的原子序数之和为37。试回答: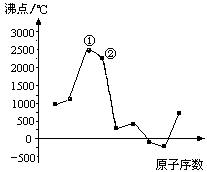 ⑵在A、B、D、E四种元素的最简单氢化物中,沸点最高的是_________(填化学式),由D、E两种元素组成的化合物属于__________晶体。
⑵在A、B、D、E四种元素的最简单氢化物中,沸点最高的是_________(填化学式),由D、E两种元素组成的化合物属于__________晶体。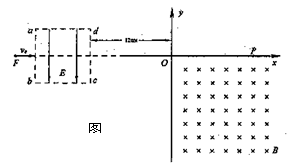 (18分) 如图14所示,正方形区域abcd的边长L=8cm,内有方向沿y轴负方向的匀强电场,场强E=3750V/m。一带电量q=+10-10C、质量m=10-20kg的微粒,以初速度v0=2×106m/s沿电场中心线FO(与x轴重合)射入电场,微粒经过边界cd飞出电场,后又进入垂直于纸面向内的匀强磁场区域(分布在坐标系第IV象限,足够大),开始做匀速圆周运动。已知cd到y轴的距离为12cm,不计微粒重力。试求:
(18分) 如图14所示,正方形区域abcd的边长L=8cm,内有方向沿y轴负方向的匀强电场,场强E=3750V/m。一带电量q=+10-10C、质量m=10-20kg的微粒,以初速度v0=2×106m/s沿电场中心线FO(与x轴重合)射入电场,微粒经过边界cd飞出电场,后又进入垂直于纸面向内的匀强磁场区域(分布在坐标系第IV象限,足够大),开始做匀速圆周运动。已知cd到y轴的距离为12cm,不计微粒重力。试求: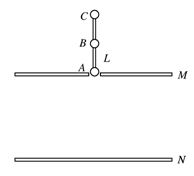 (18分)如图所示,一带电平行板电容器水平放置,金属板M上开有一小孔。有A、B、C三个质量均为m、电荷量均为+q的带电小球(可视为质点),其间用长为L的绝缘轻杆相连,处于竖直状态。已知M、N两板间距为3L,现使A小球恰好位于小孔中,由静止释放并让三个带电小球保持竖直下落,当A球到达N极板时速度刚好为零,求:
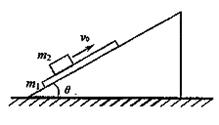
(18分)如图所示,一带电平行板电容器水平放置,金属板M上开有一小孔。有A、B、C三个质量均为m、电荷量均为+q的带电小球(可视为质点),其间用长为L的绝缘轻杆相连,处于竖直状态。已知M、N两板间距为3L,现使A小球恰好位于小孔中,由静止释放并让三个带电小球保持竖直下落,当A球到达N极板时速度刚好为零,求: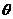 的光滑斜面上放有一个质量为m1的长木板,当质量为m2的物块以初速度v0在木板上平行于斜面向上滑动时,木板恰好相对斜面体静止,已知物块在木板上滑的整个过程中,斜面体相对地面没有滑动。求:
的光滑斜面上放有一个质量为m1的长木板,当质量为m2的物块以初速度v0在木板上平行于斜面向上滑动时,木板恰好相对斜面体静止,已知物块在木板上滑的整个过程中,斜面体相对地面没有滑动。求: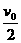 时所通过的距离。
时所通过的距离。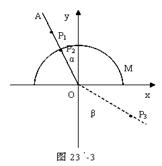 [1].(6分)如图23'-3,画有直角坐标系Oxy的白纸位于水平桌面上,M是放在白纸上的半圆形玻璃砖,其底面的圆心在坐标的原点,直边与x轴重合,OA是画在纸上的直线,P1 、P2为竖直地插在直线OA上的两枚大头针,P3 是竖直地插在纸上的第三枚大头针,α是直线OA与y轴正方向的夹角,β是直线OP3与轴负方向的夹角,只要直线OA画得合适,且P3的位置取得正确,测得角α和β,便可求得玻璃的折射率。
[1].(6分)如图23'-3,画有直角坐标系Oxy的白纸位于水平桌面上,M是放在白纸上的半圆形玻璃砖,其底面的圆心在坐标的原点,直边与x轴重合,OA是画在纸上的直线,P1 、P2为竖直地插在直线OA上的两枚大头针,P3 是竖直地插在纸上的第三枚大头针,α是直线OA与y轴正方向的夹角,β是直线OP3与轴负方向的夹角,只要直线OA画得合适,且P3的位置取得正确,测得角α和β,便可求得玻璃的折射率。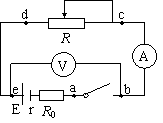 [2](12分)某同学在用电流表和电压表测电池的电动势和内阻的实验中,串联了一只2.5Ω的保护电阻R0,实验电路如图所示,
[2](12分)某同学在用电流表和电压表测电池的电动势和内阻的实验中,串联了一只2.5Ω的保护电阻R0,实验电路如图所示,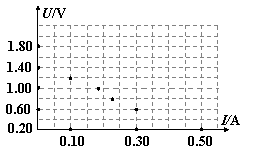
 (2)排除故障后,该同学顺利完成实验,测定下列数据根据数据在下面坐标图中画出U-I图,由图知:电池的电动势为
(2)排除故障后,该同学顺利完成实验,测定下列数据根据数据在下面坐标图中画出U-I图,由图知:电池的电动势为