28.(8分)在实验探究课上,老师给了同学们一包红色粉末,该粉末是铜粉和氧化铁(Fe2O3) 粉末中的一种或两种。同学们为了确定该粉末的成份,进行如下探究。请你参与他们的探究活动并回答问题。
(1)[提出问题] 假设1:红色粉末是铜粉;假设2:红色粉末是氧化铁粉;假设3:红色粉末是 。
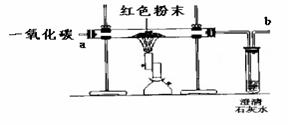 (2)[设计实验方案] 同学们为了验证上述假设,设计了如下图实验装置,并对实验结果作了如下设想和分析:取少量红色粉末放入硬质玻璃管中,通入一氧化碳,片刻后加热至充分反应。
(2)[设计实验方案] 同学们为了验证上述假设,设计了如下图实验装置,并对实验结果作了如下设想和分析:取少量红色粉末放入硬质玻璃管中,通入一氧化碳,片刻后加热至充分反应。
请完成下表:
|
实验中可能出现的现象 |
结论 |
|
|
则假设1成立 |
|
|
则假设2成立 |
|
|
则假设3成立 |
(3)[进行实验]通过实验,确认假设3成立。
(4)[反思与评价]
①实验过程中,硬质玻璃管内发生反应的化学反应方程式是:
②实验时,先通入一氧化碳片刻后再加热的原因是:
 ③从环保的角度看,上面的实验装置有不足之处,请你对该装置进行改进,具体措施是:
③从环保的角度看,上面的实验装置有不足之处,请你对该装置进行改进,具体措施是:
。
27.(9分)某化学兴趣小组的同学设计了如下图所示实验装置,进行气体的制取与收集实验。
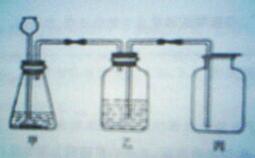
(1)上述装置有一处设计明显错误,请改正: 。
(2)用改正的装置进行如下实验:
①李军同学想利用该装置制取和收集干燥纯净的氧气,写出甲中发生反应的化学方程式:
。乙中应盛放的试剂是:
检验气体是否集满的方法是 。
②小芳和小明想利用上述装置制取干燥的CO2,请对他们的方案给予评价。
|
学生 |
制取的气体 |
甲中盛放的试剂 |
乙中盛放的仪器 |
评价 |
|
小芳 |
CO2 |
大理石和稀硫酸 |
浓硫酸 |
|
|
小明 |
CO2 |
大理石与稀盐酸 |
浓氢氧化钠溶液 |
|
23.(9分)金属活动性顺序是初中化学中的重要内容,某化学学习小组学完该内容后对其进行了进一步的总结。请你根据下列要求填空。
(1)金属与酸(稀硫酸、稀盐酸)反应的类型是 反应(从“化合”、“分解”、“置换”、“复分解”中选择),发生反应的规律是:
。
(2)金属钛是航空、军工、电力等工业领域的重要材料,地壳中的含钛矿石之一是金红石(TiO2)。目前大规模生产钛的方法是:使金红石与碳粉混合,在高温下反应,同时通入氯气(Cl2),制得TiCl4和一种可燃性气体。该反应的化学方程式是 。然后在隔绝空气、高温条件下,用过量的金属镁跟TiCl4反应制得金属钛。写出该反应的化学方程式: 。
(3)该化学学习小组想要探究铝和钛的活动性顺序,进行了如下实验:
①先用砂纸将大小薄厚相同的两种金属片表面擦光亮;②然后分别放入盛有相同的溶质质量分数、相同体积盐酸的试管中,观察到下列现象:
|
金属 |
铝 |
钛 |
|
实验现象 |
放出气泡快 |
放出气泡缓慢 |
从上表现象推断两种金属的活动性顺序是 。金属钛
(填“能”或“不能”)与硫酸铜溶液发生置换反应,原因是:
。
 (8分)从下图所示的实验仪器中,选择相关的仪器,按要求填写下列空白:
(8分)从下图所示的实验仪器中,选择相关的仪器,按要求填写下列空白: