摘要: 宇宙中元素含量最高的是 ( ) A. H元素 B. C元素 C. O元素 D. He元素
网址:http://m.1010jiajiao.com/timu3_id_350330[举报]
现有五种短周期主族元素A、B、C、D、E,其原子序数依次增大.A原子约占宇宙中原子总数的88 6%,A+又称为质子:B是形成化合物种类最多的元素,C元素的最简单的氢化物Y的水溶液显碱性.E是短周期元素中电负性最小的元素.A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物.试回答下列问题:
(1)写出A、E两元素形成的原子个数比为1:1的化合物的电子式 .
(2)向氯化亚铁溶液滴加过量的E的最高价氧化物对应水化物的溶液,现象是 .
(3)Y溶液显碱性的原因是(用一个离子方程式表示) .
(4)检验汽车尾气中含有的化合物BD的方法是:向酸性PdCl2溶液中通A汽车尾气,若生成黑色沉淀(Pd),证明汽车尾气中含有BD.写出反应的离子方程式 .
(5)下列有关物质性质的比较中.不正确的是 .
a.热稳定性:H2S>SiH4 b.离子半径:Na+>S2-
c.第一电离能N>O d.元素电负性:C>H
(6)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ/mol
②CH3OH(g)+
O2(g)=CO2(g)+2H2O(g)△H=-192.9kJ/mol
由上述方程式可知.CH3OH的燃烧热 (填“大于”、“等于”或小于”)192.9kJ/mol.已知水的气化热为44kJ/mol.则表示氢气燃烧热的热化学方程式为 .
查看习题详情和答案>>
(1)写出A、E两元素形成的原子个数比为1:1的化合物的电子式
(2)向氯化亚铁溶液滴加过量的E的最高价氧化物对应水化物的溶液,现象是
(3)Y溶液显碱性的原因是(用一个离子方程式表示)
(4)检验汽车尾气中含有的化合物BD的方法是:向酸性PdCl2溶液中通A汽车尾气,若生成黑色沉淀(Pd),证明汽车尾气中含有BD.写出反应的离子方程式
(5)下列有关物质性质的比较中.不正确的是
a.热稳定性:H2S>SiH4 b.离子半径:Na+>S2-
c.第一电离能N>O d.元素电负性:C>H
(6)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ/mol
②CH3OH(g)+
| 3 | 2 |
由上述方程式可知.CH3OH的燃烧热
A、B、C、D、E、F六种短周期元素的原子序数依次增大.A是宇宙中含量最丰元素,B元素的原子价电子排布为nsnnpn,D元素的最外层电子数是其电子层数的3倍,F的最高价氧化物对应水化物有两性,能溶于C、E的最高价氧化物对应水化物中.试回答:
(1)写出C原子的价层电子轨道表示式: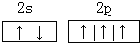
 ;D原子的价层电子排布式:
;D原子的价层电子排布式: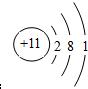
 ;
;
(2)B位于元素周期表的第
(3)C的基态原子核外有
(4)E单质在空气中燃烧生成物的电子式: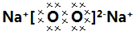
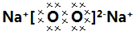 ,其中的阳离子与阴离子的个数比是
,其中的阳离子与阴离子的个数比是
(5)F的固态氧化物的用途有
查看习题详情和答案>>
(1)写出C原子的价层电子轨道表示式:


2s22p4
2s22p4
,E的原子结构示意图:

(2)B位于元素周期表的第
IVA
IVA
族,A、B形成原子个数比1:1且直线形分子的结构式:H-C≡C-H
H-C≡C-H
;(3)C的基态原子核外有
7
7
种不同运动状态的电子;(4)E单质在空气中燃烧生成物的电子式:
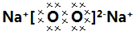
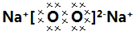
2:1
2:1
;(5)F的固态氧化物的用途有
耐火材料
耐火材料
(说出一种).F的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的两种化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用),其反应的化学方程式是4Al+3TiO2+3C
2Al2O3+3TiC
| ||
4Al+3TiO2+3C
2Al2O3+3TiC
.
| ||
A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
|
元素 |
相关信息 |
|
A |
原子核外有6种不同运动状态的电子 |
|
C |
基态原子中s电子总数与p电子总数相等 |
|
D |
原子半径在同周期元素中最大 |
|
E |
基态原子最外层电子排布式为3s23p1 |
|
F |
基态原子的最外层p轨道有两个电子的自旋方向与其它电子的自旋方向相反 |
|
G |
基态原子核外有7个能级且能量最高的能级上有6个电子 |
|
H |
是我国使用最早的合金中的最主要元素 |
请用化学用语填空:
(1)A元素位于元素周期表第 周期 族,B元素和C元素的第一电离能比较,较大的是 ,C元素和F元素的电负性比较,较小的是 。
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的分子构型为 ,
B元素所形成的单质分子中σ键与π键数目之比为 。
(3)G元素的低价阳离子的离子结构示意图是_____________,F元素原子的价电子构型的电子排布图(轨道表示式)是__________________,H元素的基态原子核外电子排布式是 。
(4)G的高价阳离子的溶液与H单质反应的离子方程式为 ;
与E元素成对角关系的某元素的最高价氧化物的水化物具有两性,写出该两性物质与D元素的最高价氧化物的水化物反应的化学方程式为 。
查看习题详情和答案>>
A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
| 元素 | 相关信息 |
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子最外层电子排布式为3s23p1 |
| F | 基态原子的最外层p轨道有两个电子的自旋方向与其它电子的自旋方向相反 |
| G | 基态原子核外有7个能级且能量最高的能级上有6个电子 |
| H | 是我国使用最早的合金中的最主要元素 |
请用化学用语填空:
(1)A元素位于元素周期表第 周期 族,B元素和C元素的第一电离能比较,较大的是 ,C元素和F元素的电负性比较,较小的是 。
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的分子构型为 ,
B元素所形成的单质分子中σ键与π键数目之比为 。
(3)G元素的低价阳离子的离子结构示意图是_____________,F元素原子的价电子构型的电子排布图(轨道表示式)是__________________,H元素的基态原子核外电子排布式是 。
(4)G的高价阳离子的溶液与H单质反应的离子方程式为 ;
与E元素成对角关系的某元素的最高价氧化物的水化物具有两性,写出该两性物质与D元素的最高价氧化物的水化物反应的化学方程式为 。 查看习题详情和答案>>
A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
请用化学用语填空:
(1)A元素位于元素周期表第 周期 族,B元素和C元素的第一电离能比较,较大的是 ,C元素和F元素的电负性比较,较小的是 。
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的分子构型为 ,
B元素所形成的单质分子中σ键与π键数目之比为 。
(3)G元素的低价阳离子的离子结构示意图是_____________,F元素原子的价电子构型的电子排布图(轨道表示式)是__________________,H元素的基态原子核外电子排布式是 。
(4)G的高价阳离子的溶液与H单质反应的离子方程式为 ;
与E元素成对角关系的某元素的最高价氧化物的水化物具有两性,写出该两性物质与D元素的最高价氧化物的水化物反应的化学方程式为 。
| 元素 | 相关信息 |
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子最外层电子排布式为3s23p1 |
| F | 基态原子的最外层p轨道有两个电子的自旋方向与其它电子的自旋方向相反 |
| G | 基态原子核外有7个能级且能量最高的能级上有6个电子 |
| H | 是我国使用最早的合金中的最主要元素 |
请用化学用语填空:
(1)A元素位于元素周期表第 周期 族,B元素和C元素的第一电离能比较,较大的是 ,C元素和F元素的电负性比较,较小的是 。
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的分子构型为 ,
B元素所形成的单质分子中σ键与π键数目之比为 。
(3)G元素的低价阳离子的离子结构示意图是_____________,F元素原子的价电子构型的电子排布图(轨道表示式)是__________________,H元素的基态原子核外电子排布式是 。
(4)G的高价阳离子的溶液与H单质反应的离子方程式为 ;
与E元素成对角关系的某元素的最高价氧化物的水化物具有两性,写出该两性物质与D元素的最高价氧化物的水化物反应的化学方程式为 。