题目内容
A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
请用化学用语填空:
(1)A元素位于元素周期表第 周期 族,B元素和C元素的第一电离能比较,较大的是 ,C元素和F元素的电负性比较,较小的是 。
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的分子构型为 ,
B元素所形成的单质分子中σ键与π键数目之比为 。
(3)G元素的低价阳离子的离子结构示意图是_____________,F元素原子的价电子构型的电子排布图(轨道表示式)是__________________,H元素的基态原子核外电子排布式是 。
(4)G的高价阳离子的溶液与H单质反应的离子方程式为 ;
与E元素成对角关系的某元素的最高价氧化物的水化物具有两性,写出该两性物质与D元素的最高价氧化物的水化物反应的化学方程式为 。
| 元素 | 相关信息 |
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子最外层电子排布式为3s23p1 |
| F | 基态原子的最外层p轨道有两个电子的自旋方向与其它电子的自旋方向相反 |
| G | 基态原子核外有7个能级且能量最高的能级上有6个电子 |
| H | 是我国使用最早的合金中的最主要元素 |
请用化学用语填空:
(1)A元素位于元素周期表第 周期 族,B元素和C元素的第一电离能比较,较大的是 ,C元素和F元素的电负性比较,较小的是 。
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的分子构型为 ,
B元素所形成的单质分子中σ键与π键数目之比为 。
(3)G元素的低价阳离子的离子结构示意图是_____________,F元素原子的价电子构型的电子排布图(轨道表示式)是__________________,H元素的基态原子核外电子排布式是 。
(4)G的高价阳离子的溶液与H单质反应的离子方程式为 ;
与E元素成对角关系的某元素的最高价氧化物的水化物具有两性,写出该两性物质与D元素的最高价氧化物的水化物反应的化学方程式为 。
(1)二 ⅣA, N, Cl (每空1分)
(2)三角锥形, 1:2 (每空1分)
(3)
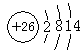
 (3s、3p未注明也得分)
(3s、3p未注明也得分)1s22s22p63s23p63d104s1 或 [Ar] 3d104s1 (每空1分)
(4)2Fe3++Cu=2Fe2++Cu2+, Be(OH)2+2NaOH=Na2BeO2+2H2O(每空2分)
试题分析:A的原子核外有6种不同运动状态的电子,即核外共有6个电子,A为碳元素。C的基态原子中s电子总数与p电子总数相等,则核外电子排布为1s22s22p4,C是氧元素。由于A、B、C原子序数依次递增,故B是氮元素。D的原子半径在同周期元素中最大,故D应为第三周期元素,是钠元素。E的基态原子最外层电子排布式为3s23p1,是铝元素。F的基态原子的最外层p轨道有两个电子的自旋方向与其它电子的自旋方向相反,说明p轨道上有5个电子,是氯元素。G的基态原子核外有7个能级且能量最高的能级上有6个电子,则其电子排布式为1s22s22p63s23p64s23d6,是铁元素。H是我国使用最早的合金中的最主要元素,是铜元素。

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
 Fe + 2ZG 放电时,电池的正极反应式为: 该电池的电解质为___________________。
Fe + 2ZG 放电时,电池的正极反应式为: 该电池的电解质为___________________。
 说法正确的是
说法正确的是 互为同素异形体
互为同素异形体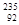 U是一种重要的核燃料,这里的“235”是指该原子的
U是一种重要的核燃料,这里的“235”是指该原子的