摘要:+CO+CO2(g) 的平衡常数K=0.5.若起始浓度c(CO) = 0.05 mol·L-1.c(CO2) = 0.01 mol·L-1.请回答: (1)判断化学反应进行的方向并计算反应物.生成物的平衡浓度. (2)CO的转化率是多少? (3)增加的FeO量会不会促使平衡向正方向移动?
网址:http://m.1010jiajiao.com/timu3_id_299745[举报]
已知反应FeO(s)+CO(g)![]() Fe(s)+CO2(g)的Kc=0.5(1 273 K)。若起始浓度c(CO)=0.05 mol·L-1,c(CO2)=0.01 mol·L-1,请回答:
Fe(s)+CO2(g)的Kc=0.5(1 273 K)。若起始浓度c(CO)=0.05 mol·L-1,c(CO2)=0.01 mol·L-1,请回答:
(1)判断化学反应进行的方向并计算反应物、生成物的平衡浓度。
(2)CO的转化率是多少?
(3)增加FeO的量,对平衡有无影响?
查看习题详情和答案>>已知反应FeO(s)+CO(g) = Fe(s)+CO2(g) 的平衡常数K=0.5(1273K)。若起始浓度c(CO)= 0.05 mol·L-1,c(CO2) = 0.01 mol·L-1,请回答:
(1)判断化学反应进行的方向并计算反应物、生成物的平衡浓度。
(2)CO的转化率是多少?
(3)增加的FeO量会不会促使平衡向正方向移动?
查看习题详情和答案>>
已知反应FeO(s)+CO(g) = Fe(s)+CO2(g) 的平衡常数K=0.5(1273K)。若起始浓度c(CO) = 0.05 mol·L-1,c(CO2) = 0.01 mol·L-1,请回答:
(1)判断化学反应进行的方向并计算反应物、生成物的平衡浓度。
(2)CO的转化率是多少?
(3)增加的FeO量会不会促使平衡向正方向移动?
查看习题详情和答案>>
 Fe(s)+CO2(g) 的Kc=0.5(1273K)。若起始浓度c(CO) = 0.05 mol·L-1,c(CO2) = 0.01 mol·L-1,请回答:
Fe(s)+CO2(g) 的Kc=0.5(1273K)。若起始浓度c(CO) = 0.05 mol·L-1,c(CO2) = 0.01 mol·L-1,请回答: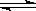 Fe(s)+CO2(g)
的Kc=0.5(1273K)。若起始浓度c(CO) = 0.05 mol·L-1,c(CO2) = 0.01 mol·L-1,请回答:
Fe(s)+CO2(g)
的Kc=0.5(1273K)。若起始浓度c(CO) = 0.05 mol·L-1,c(CO2) = 0.01 mol·L-1,请回答: