题目内容
已知反应FeO(s)+CO(g)![]() Fe(s)+CO2(g)的Kc=0.5(1 273 K)。若起始浓度c(CO)=0.05 mol·L-1,c(CO2)=0.01 mol·L-1,请回答:
Fe(s)+CO2(g)的Kc=0.5(1 273 K)。若起始浓度c(CO)=0.05 mol·L-1,c(CO2)=0.01 mol·L-1,请回答:
(1)判断化学反应进行的方向并计算反应物、生成物的平衡浓度。
(2)CO的转化率是多少?
(3)增加FeO的量,对平衡有无影响?
(1)反应向右进行;反应物(CO)、生成物(CO2)的平衡浓度分别为0.04 mol·L-1、0.02 mol·L-1。(2)20% (3)无影响
解析:
![]()
Qc<Kc,反应将向右进行,设平衡时CO2增加的浓度为x mol·L-1,则平衡时:
FeO(s)+CO(g)![]() Fe(s)+CO2(g)?
Fe(s)+CO2(g)?
![]() 0.05-x 0.01+x
0.05-x 0.01+x
![]()
解之,x=0.01 mol·L-1
[CO]=0.05 mol·L-1-0.01 mol·L-1=0.04 mol·L-1
[CO2]=0.01 mol·L-1+0.01 mol·L-1=0.02 mol·L-1
![]()
答:CO和CO2的平衡浓度分别为0.04 mol·L-1、0.02 mol·L-1;CO的转化率为20%;增加FeO的量,对平衡无影响。

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案
相关题目
 Fe(s)+CO2(g) 的Kc=0.5(1273K)。若起始浓度c(CO) = 0.05 mol·L-1,c(CO2) = 0.01 mol·L-1,请回答:
Fe(s)+CO2(g) 的Kc=0.5(1273K)。若起始浓度c(CO) = 0.05 mol·L-1,c(CO2) = 0.01 mol·L-1,请回答: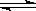 Fe(s)+CO2(g)
的Kc=0.5(1273K)。若起始浓度c(CO) = 0.05 mol·L-1,c(CO2) = 0.01 mol·L-1,请回答:
Fe(s)+CO2(g)
的Kc=0.5(1273K)。若起始浓度c(CO) = 0.05 mol·L-1,c(CO2) = 0.01 mol·L-1,请回答: