摘要: 反应MnO2+4HCl△===MnCl2+Cl2↑+2H2O中.盐酸的作用是 A. 只作酸 B. 只作还原剂 C. 既作酸.又作氧化剂 D. 既作酸.又作还原剂
网址:http://m.1010jiajiao.com/timu3_id_205895[举报]
(Ⅰ)实验室中盐酸的用途十分广泛,常常用来制备气体.
(1)某小组同学欲用4mol/L的盐酸配制230mL 0.4mol/L 盐酸溶液,需取用4mol/L盐酸
(2)下列实验操作使配制的溶液浓度偏低的是
A.容量瓶洗涤后未干燥
B.移液时,有少量溶液溅出
C.定容时,加水不慎超过刻度线,又倒出一些
D.定容时,俯视刻度线
E.装入试剂瓶时,有少量溶液溅出
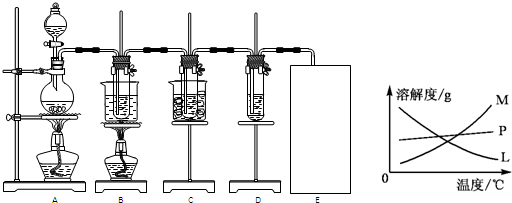
(Ⅱ)瑞典化学家舍勒将软锰矿(主要成分为MnO2)与浓盐酸混合加热,在世界上首先得到了氯气.已知Cl2和碱溶液在不同条件下,得到的产物不同,某兴趣小组用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质.( 3Cl2+6KOH
KClO3+5KCl+3H2O )图中:A为氯气发生装置;B的试管里盛有15mL 30% KOH溶液,并置于水浴中;C的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;D的试管里加有紫色石蕊试液.
请填写下列空白:
(1)制取氯气时,在圆底烧瓶里加入一定质量的二氧化锰,通过
(2)反应完毕经冷却后,B的试管中有大量晶体析出.图中符合该晶体溶解度曲线的是
(3)实验中可观察到D的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
(4)请在装置图方框中画出缺少的实验装置,并注明试剂.
查看习题详情和答案>>

(1)某小组同学欲用4mol/L的盐酸配制230mL 0.4mol/L 盐酸溶液,需取用4mol/L盐酸
25
25
mL,实验中需要用到的玻璃仪器有烧杯
烧杯
、250ml容量瓶
250ml容量瓶
、量筒、烧杯、胶头滴管.(2)下列实验操作使配制的溶液浓度偏低的是
BC
BC
A.容量瓶洗涤后未干燥
B.移液时,有少量溶液溅出
C.定容时,加水不慎超过刻度线,又倒出一些
D.定容时,俯视刻度线
E.装入试剂瓶时,有少量溶液溅出
(Ⅱ)瑞典化学家舍勒将软锰矿(主要成分为MnO2)与浓盐酸混合加热,在世界上首先得到了氯气.已知Cl2和碱溶液在不同条件下,得到的产物不同,某兴趣小组用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质.( 3Cl2+6KOH
| ||
请填写下列空白:
(1)制取氯气时,在圆底烧瓶里加入一定质量的二氧化锰,通过
分液漏斗
分液漏斗
(填仪器名称)向圆底烧瓶中加入适量的浓盐酸.装置A中反应的离子方程式MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
.
| ||
(2)反应完毕经冷却后,B的试管中有大量晶体析出.图中符合该晶体溶解度曲线的是
M
M
(填编号字母);从B的试管中分离出该晶体的方法是过滤
过滤
(填实验操作名称).该小组同学发现制得的氯酸钾产量偏低,可能的一种原因是Cl2中含有杂质,该杂质成分HCl
HCl
(除水蒸气外,填化学式),如何改进AB间增加一个盛有饱和氯化钠溶液吸收氯化氢的洗气装置
AB间增加一个盛有饱和氯化钠溶液吸收氯化氢的洗气装置
;(3)实验中可观察到D的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为 红 红 色 |
氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成的HClO将石蕊氧化为无色物质 氯气与水反应生成的HClO将石蕊氧化为无色物质 |
瑞典化学家舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色、刺激性气味的气体氯气.某学生使用这一原理设计如图所示的实验装置,并且利用制得的氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:

(1)A仪器的名称是
(2)漂白粉将在U形管中产生,其化学方程式是
(3)此实验结果所得Ca(ClO)2产率太低.经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是
②试判断另一个副反应(写出此反应方程式):
(4)漂粉精同盐酸作用产生氯气:Ca(ClO)2+4HCl=2Cl2↑+CaCl2+2H2O,该反应中每生成1 mol Cl2,转移电子的物质的量为
查看习题详情和答案>>

(1)A仪器的名称是
分液漏斗
分液漏斗
,所盛试剂是浓盐酸
浓盐酸
,B中发生反应的化学方程式是MnO2+4HCl(浓)
MnCl2+2H2O+Cl2↑
| ||
MnO2+4HCl(浓)
MnCl2+2H2O+Cl2↑
.
| ||
(2)漂白粉将在U形管中产生,其化学方程式是
2Cl2 +2Ca(OH)2=CaCl2 +Ca(ClO)2 +2H2O
2Cl2 +2Ca(OH)2=CaCl2 +Ca(ClO)2 +2H2O
.(3)此实验结果所得Ca(ClO)2产率太低.经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是
将U形管置于冷水浴中
将U形管置于冷水浴中
.②试判断另一个副反应(写出此反应方程式):
2HCl+Ca(OH)2=CaCl2+2H2O
2HCl+Ca(OH)2=CaCl2+2H2O
.为避免此副反应发生,应采取的措施是在B、C之间增加一个饱和食盐水洗气装置
在B、C之间增加一个饱和食盐水洗气装置
.(4)漂粉精同盐酸作用产生氯气:Ca(ClO)2+4HCl=2Cl2↑+CaCl2+2H2O,该反应中每生成1 mol Cl2,转移电子的物质的量为
1
1
mol,被氧化的HCl的物质的量为1
1
mol.有效氯是漂粉精中有效Ca(ClO)2 的含量大小的标志.已知:有效氯=(漂粉精加盐酸所释放出的氯气的质量/漂粉精的质量)×100%,该漂粉精的有效氯为65%,则该漂粉精中Ca(ClO)2的质量分数为65.5%
65.5%
(保留一位小数).如图是用干燥纯净的Cl2与Cu粉反应来制取无水氯化铜的装置图,请回答下列问题:

(1)小试管的作用是
(2)B瓶中的溶液是
(3)干燥管E中盛有碱石灰,其作用是
(4)开始实验时,应先点燃
查看习题详情和答案>>

(1)小试管的作用是
液封
液封
;烧瓶中发生反应的化学方程式是MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
;
| ||
(2)B瓶中的溶液是
饱和食盐水
饱和食盐水
,C瓶中盛放的溶液是浓硫酸
浓硫酸
.(3)干燥管E中盛有碱石灰,其作用是
吸收未反应完的Cl2,防止空气中的水蒸气进入反应装置
吸收未反应完的Cl2,防止空气中的水蒸气进入反应装置
.(4)开始实验时,应先点燃
A
A
处(填“A”或“D”)的酒精灯,当D中充满黄绿色的气体后
D中充满黄绿色的气体后
时再点燃另一处的酒精灯.实验室中用二氧化锰跟浓盐酸反应制取氯气,反应的化学方程式为
全部被还原成Mn2+,当用高锰酸钾跟浓盐酸在室温下反应制取氯气,反应中有5mol e-转移时,可得到氯气
查看习题详情和答案>>
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
.常被用作制取氧气的高猛酸钾是常用的氧化剂,在酸性条件下,Mn
| ||
| O | - 4 |
56
56
L(标准状况).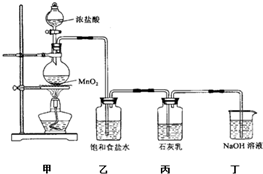 某兴趣小组设计了下列实验装置探究氯气与石灰乳反应的条件和产物.
某兴趣小组设计了下列实验装置探究氯气与石灰乳反应的条件和产物.(1)装置甲中反应的化学方程式是
MnO2+4HCl
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl
MnCl2+Cl2↑+2H2O
.
| ||
(2)乙装置的作用是
除去氯气中混有的氯化氢
除去氯气中混有的氯化氢
,丁装置的作用是吸收Cl2防止污染空气
吸收Cl2防止污染空气
.(3)该兴趣小组用100mL 12mol?L-1盐酸与8.7g MnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可制得Ca(ClO)2
7.15
7.15
g.(请写出必要的计算过程)(4)已知:氯气和碱的反应为放热反应(即随着反应的进行有热量放出,导致体系温度逐渐升高),温度较高时,氯气和碱还能发生如下反应:
3Cl2+6NaOH
| ||
将丙装置浸在盛有冷水的水槽中
将丙装置浸在盛有冷水的水槽中
.