��Ŀ����
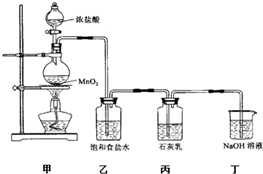
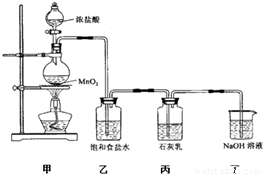
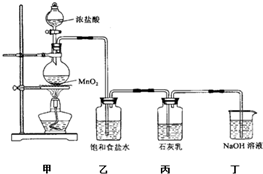 ij��ȤС�����������ʵ��װ��̽��������ʯ���鷴Ӧ�������Ͳ��
ij��ȤС�����������ʵ��װ��̽��������ʯ���鷴Ӧ�������Ͳ����1��װ�ü��з�Ӧ�Ļ�ѧ����ʽ��
MnO2+4HCl
MnCl2+Cl2��+2H2O
| ||
MnO2+4HCl
MnCl2+Cl2��+2H2O
��
| ||
��2����װ�õ�������
��ȥ�����л��е��Ȼ���
��ȥ�����л��е��Ȼ���
����װ�õ�����������Cl2��ֹ��Ⱦ����
����Cl2��ֹ��Ⱦ����
����3������ȤС����100mL 12mol?L-1������8.7g MnO2�Ʊ��������������������������ʯ���鷴Ӧ���������������Ƶ�Ca��ClO��2
7.15
7.15
g������д����Ҫ�ļ�����̣���4����֪�������ͼ�ķ�ӦΪ���ȷ�Ӧ�������ŷ�Ӧ�Ľ����������ų���������ϵ�¶������ߣ����¶Ƚϸ�ʱ�������ͼ�ܷ������·�Ӧ��
3Cl2+6NaOH
| ||
����װ�ý���ʢ����ˮ��ˮ����
����װ�ý���ʢ����ˮ��ˮ����
����������1��װ�ü��������ķ���װ�ã�����������Ũ�����ڼ��ȵ������·�Ӧ�����Ȼ��̡�������ˮ��
��2���Ȼ����ӷ�����ȡ�������к���HCl��Ӱ��������Ӧ�����̽����
ʵ��β���к���δ��Ӧ�������������ж���ֱ���ſգ�����Ⱦ����������������������Һ���գ�
��3�����ݹ��������ж����ᡢ������������һ��ʣ�࣬���ݲ�������ʼ������ɵ��������ڸ��ݷ���ʽ�������ɵ�
Ca��ClO��2������
��4������Ŀ��Ϣ��֪�������ͼ�ķ�ӦΪ���ȷ�Ӧ���¶ȹ��ߣ������ͼӦ�����������Σ����´������εIJ��ʽ��ͣ���Ӧ����װ�����ڵ��»�����
��2���Ȼ����ӷ�����ȡ�������к���HCl��Ӱ��������Ӧ�����̽����
ʵ��β���к���δ��Ӧ�������������ж���ֱ���ſգ�����Ⱦ����������������������Һ���գ�
��3�����ݹ��������ж����ᡢ������������һ��ʣ�࣬���ݲ�������ʼ������ɵ��������ڸ��ݷ���ʽ�������ɵ�
Ca��ClO��2������
��4������Ŀ��Ϣ��֪�������ͼ�ķ�ӦΪ���ȷ�Ӧ���¶ȹ��ߣ������ͼӦ�����������Σ����´������εIJ��ʽ��ͣ���Ӧ����װ�����ڵ��»�����
����⣺��1������������Ũ�����ڼ��ȵ������·�Ӧ�����Ȼ��̡�������ˮ��
��Ӧ����ʽΪ��MnO2+4HCl
MnCl2+Cl2��+2H2O��
�ʴ�Ϊ��MnO2+4HCl
MnCl2+Cl2��+2H2O��
��2���Ȼ����ӷ�����ȡ�������к���HCl��Ӱ��������Ӧ�����̽�����ñ���ʳ��ˮ��ȥ�����л��е��Ȼ��⣻
ʵ��β���к���δ��Ӧ�������������ж���ֱ���ſգ�����Ⱦ����������������������Һ���գ�
�ʴ�Ϊ����ȥ�����л��е��Ȼ��⣻����Cl2��ֹ��Ⱦ������
��3��8.7gMnO2�����ʵ���Ϊ
=0.1mol�����ݷ���ʽMnO2+4HCl
MnCl2+Cl2��+2H2O��֪��MnO2��ȫ��Ӧ��ҪHCl�����ʵ���Ϊ0.4mol��С��0.1L��12mol?L-1=1.2mol���ʶ���������ȫ��Ӧ���ɷ���ʽ��֪��������0.1mol���ɷ���ʽ2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O��֪��0.1mol������ȫ��Ӧ����0.05molCa��ClO��2��
����Ϊ0.05mol��143g��mol=7.15g��
�ʴ�Ϊ��7.15g��
��4������Ŀ��Ϣ��֪�������ͼ�ķ�ӦΪ���ȷ�Ӧ���¶ȹ��ߣ������ͼӦ�����������Σ����´������εIJ��ʽ��ͣ����Խ���װ�ý���ʢ����ˮ��ˮ���н����¶ȣ�
�ʴ�Ϊ������װ�ý���ʢ����ˮ��ˮ���У�
��Ӧ����ʽΪ��MnO2+4HCl
| ||
�ʴ�Ϊ��MnO2+4HCl
| ||
��2���Ȼ����ӷ�����ȡ�������к���HCl��Ӱ��������Ӧ�����̽�����ñ���ʳ��ˮ��ȥ�����л��е��Ȼ��⣻
ʵ��β���к���δ��Ӧ�������������ж���ֱ���ſգ�����Ⱦ����������������������Һ���գ�
�ʴ�Ϊ����ȥ�����л��е��Ȼ��⣻����Cl2��ֹ��Ⱦ������
��3��8.7gMnO2�����ʵ���Ϊ
| 8.7g |
| 87g/mol |
| ||
����Ϊ0.05mol��143g��mol=7.15g��
�ʴ�Ϊ��7.15g��
��4������Ŀ��Ϣ��֪�������ͼ�ķ�ӦΪ���ȷ�Ӧ���¶ȹ��ߣ������ͼӦ�����������Σ����´������εIJ��ʽ��ͣ����Խ���װ�ý���ʢ����ˮ��ˮ���н����¶ȣ�
�ʴ�Ϊ������װ�ý���ʢ����ˮ��ˮ���У�
������������������ȡ�����������ʡ��Է�Ӧװ�õ����⡢��Ӧ�����Ŀ��Ƶȣ��Ѷ��еȣ�ע�⣨3���й������㣮

��ϰ��ϵ�д�
�����Ŀ
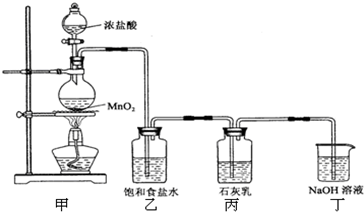
 ij��ȤС�����������ʵ��װ��̽��������ʯ���鷴Ӧ�������Ͳ��
ij��ȤС�����������ʵ��װ��̽��������ʯ���鷴Ӧ�������Ͳ�� 5NaCl+NaClO3+3H2OΪ�����Ca��ClO��2�IJ��ʣ��ɶԱ�װ�����ʵ��Ľ����������һ�ָĽ�������______��
5NaCl+NaClO3+3H2OΪ�����Ca��ClO��2�IJ��ʣ��ɶԱ�װ�����ʵ��Ľ����������һ�ָĽ�������______��