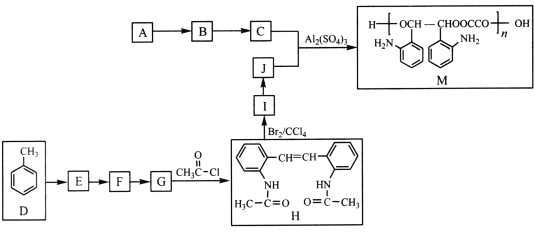
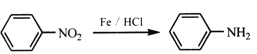
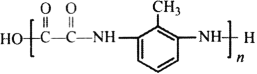
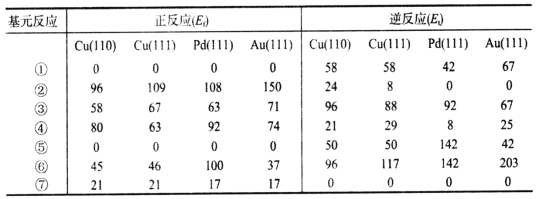
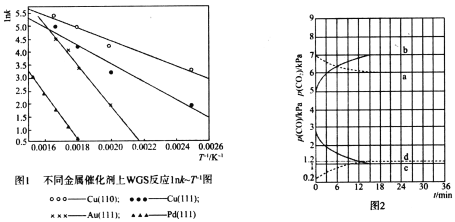
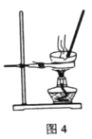
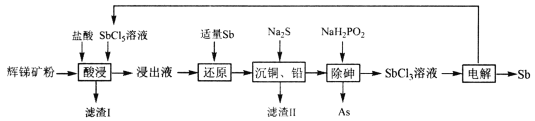
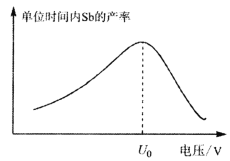
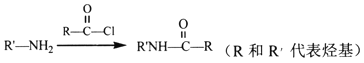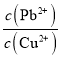【题目】某同学在用稀硫酸与锌反应制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。
(1)硫酸铜溶液可以加快氢气生成速率的原因是____。
(2)25℃,该同学设计三个实验探究影响锌粉(足量)与稀硫酸反应速率的因素,有关数据如下表所示:
实验序号 | 体积/mL | ||
1.0mol·L-1硫酸溶液 | 饱和CuSO4溶液 | 水 | |
I | 30.0 | 1.0 | 9.0 |
II | 20.0 | 1.0 | Vx |
III | 30.0 | 3.0 | 7.0 |
①本实验待测数据可以是____。
②利用实验I和实验I来探究硫酸浓度对锌粉与稀硫酸反应速率的影响,Vx=__,理由是__。
③实验I和实验III的目的是__。
(3)用排水集气法收集实验I反应放出的氢气(气体体积已折合成标准状况),实验记录如表(累计值):
时间/min | 1 | 2 | 3 | 4 | 5 | 6 |
氢气体积/mL | 60 | 140 | 252 | 420 | 510 | 540 |
①反应速率最大时间段是__min(填“0~1”、“1~2”、“2~3”、“3~4”、“4~5”或“5~6”下同),原因是____。
②反应速率最小时段是__min,原因是___。
③第2~3min时间段以稀硫酸的浓度表示的该反应速率(设溶液体积不变)是v(H2SO4)=___。
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,在稀硫酸中分别加入等体积的下列溶液,可行的是____(填字母)。
A.KNO3溶液 B.蒸馏水 C.Na2SO4溶液 D.Na2CO3溶液