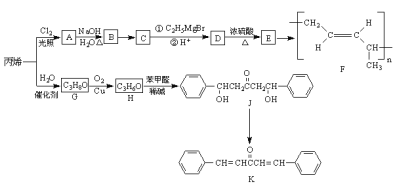
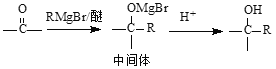
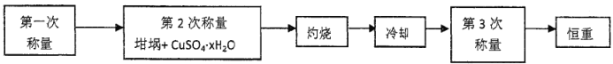
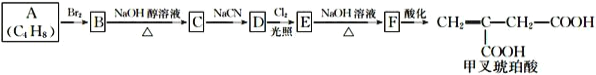
【题目】实验室用浓度为0.500mol/L的标准氢氧化钠溶液来测定未知浓度的盐酸。在锥形瓶中放入20.00mL的待测溶液,再滴加2滴酚酞,摇匀。用标准氢氧化钠溶液滴定,直到滴入最后一滴氢氧化钠溶液,指示剂的颜色_______,并在半分钟内溶液颜色不发生变化,停止滴定,记录读数。数据如表:
次数 | 滴定前(mL) | 滴定后(mL) |
1 | 0.40 | 21.10 |
2 | 0.10 |
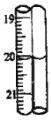
第2次滴定后滴定管的读数如图所示。根据表中的数据计算出盐酸的浓度为_____mol/L。
【题目】下列有关实验的描述正确的是( )
选项 | 实验内容 | 现象或结论 |
A | 向平衡体系FeCl3+3KSCN | 溶液颜色明显变浅 |
B | 用NaOH溶液滴定盐酸(酚酞作指示剂)至终点 | 溶液由红色变为无色 |
C | 二氧化硫通入到酸性高锰酸钾溶液中 | 酸性高锰酸钾溶液褪色,SO2具有还原性 |
D | 将钠置于一定量的乙醇中 | 钠浮在液面上剧烈反应 |
A.AB.BC.CD.D
【题目】氧化铝陶瓷常用于厚膜集成电路,制备氧化铝陶瓷的合成路线如图所示,回答下列问题。
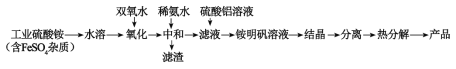
(1)“氧化”步骤发生的离子方程式为:___,使用双氧水作氧化剂优点为___:
(2)“热分解”得到的产物除了氧化铝外,还有NH3、N2、SO2、SO3、H2O生成,则氧化产物和还原产物的物质的量之比为___。
(3)铵明矾晶体的化学式为NH4Al(SO4)2·12H2O,“热分解”步骤中,其各温度段内受热“失重计算值”(失重计算值%=![]() ×100%)如表所示:
×100%)如表所示:
温度区间(℃) | 18→190 | 190→430 | 430→505 | 505→900 |
失重计算值(%) | 39.20 | 7.80 | 13.00 | 26.00 |
通过上述数据经粗略计算可判断,在温度区间___铵明矾基本上失去了全部结晶水。
(4)“结晶”步骤中常采用的操作是___。
(5)合成过程中常使用过量的工业硫酸铵,可利用硫酸铵溶液水解显酸性抑制硫酸铝水解,另外的一个重要作用是___。
(6)通常认为金属离子浓度等于1×10-5mol/L即可认为沉淀完全,试计算常温下“中和”步骤中需要调节溶液pH=___(保留一位小数,已知:Ksp[Fe(OH)3]=8.0×10-38,lg5=0.7)。