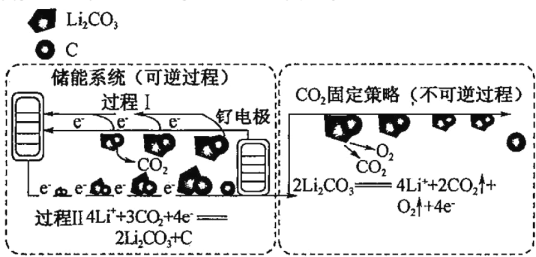
【题目】无水![]() 是一种重要的化工原料。某课外探究小组尝试制取无水
是一种重要的化工原料。某课外探究小组尝试制取无水![]() ,查阅资料获得下列信息:无水
,查阅资料获得下列信息:无水![]() 在
在![]() 升华,极易潮解,遇到水蒸气会产生白色烟雾。
升华,极易潮解,遇到水蒸气会产生白色烟雾。
探究一无水![]() 的实验室制备
的实验室制备
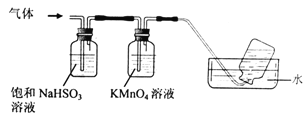
利用如图装置,用干燥、纯净的氯气在加热条件下与铝粉![]() 已除去氧化膜
已除去氧化膜![]() 反应制取无水AlCl3。供选择的药品:①铝粉②浓硫酸③稀盐酸④饱和食盐水⑤二氧化锰粉末⑥无水氯化钙⑦稀硫酸⑧浓盐酸⑨氢氧化钠溶液
反应制取无水AlCl3。供选择的药品:①铝粉②浓硫酸③稀盐酸④饱和食盐水⑤二氧化锰粉末⑥无水氯化钙⑦稀硫酸⑧浓盐酸⑨氢氧化钠溶液
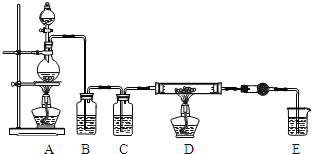
(1)写出装置A烧瓶中发生的反应方程式 ______ 。
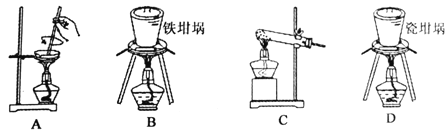
(2)实验开始前,先检查装置气密性,然后装入药品,接下来的步骤依次是 ______ ![]() 填序号
填序号![]() 。
。
![]() 加热D中硬质玻璃管
加热D中硬质玻璃管
![]() 往A烧瓶中加入液体
往A烧瓶中加入液体
![]() 点燃A中的酒精灯
点燃A中的酒精灯
(3)上述供选药品中本实验无需用到的是 ______ ![]() 填数字序号
填数字序号![]() 。
。
(4)写出无水![]() 与水蒸气反应的化学方程式 ______ 。
与水蒸气反应的化学方程式 ______ 。
探究二无水![]() 的含量测定及结果分析
的含量测定及结果分析
取D中反应后所得固体![]() ,与足量氢氧化钠溶液反应,测定生成气体的体积
,与足量氢氧化钠溶液反应,测定生成气体的体积![]() 体积均换算成标准状况
体积均换算成标准状况![]() ,重复测定三次,数据如下:
,重复测定三次,数据如下:
第一次实验 | 第二次实验 | 第三次实验 | |
D中固体用量 |
|
|
|
氢气的体积 |
|
|
|
(5)根据表中数据,计算所得固体中无水![]() 的质量分数 ______ 。
的质量分数 ______ 。
(6)有同学认为测得的无水![]() 的质量分数偏低,你认为可能的原因有 ______ 。
的质量分数偏低,你认为可能的原因有 ______ 。
探究三离子浓度对氯气制备的影响
二氧化锰粉末和浓盐酸的反应随着盐酸的浓度降低,反应停止不再产生氯气。探究小组对盐酸浓度降低影响氯气生成的原因进行如下探究:
(7)提出假设假设1:![]() 浓度降低影响氯气的生成
浓度降低影响氯气的生成
假设2: ______ 。
(8)设计方案进行实验。限选试剂:浓![]() 、NaCl固体、
、NaCl固体、![]() 固体、稀盐酸。
固体、稀盐酸。
步骤 | 实验操作 | 预测现象和结论 |
| 往不再产生氯气的装置中,加入 ______ ,继续加热 | 若有黄绿色气体生成,则假设1成立 |
| ______ | 若有黄绿色气体生成,则假设2成立 |
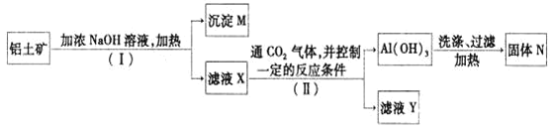
【题目】碳酸镁晶须是一种新型吸波隐形材料中的增强剂。某工厂以MgCl2(含少量杂质FeCl2、FeCl3)为原料制备碳酸镁晶须(MgCO3·H2O)的工艺流程如下:

已知:Fe3+、Fe2+、Mg2+生成氢氧化物沉淀时的pH
注:Fe(OH)2沉淀呈絮状,不易从溶液中除去。
物质 | 开始沉淀 | 沉淀完全 |
Fe(OH)3 | 2.7 | 3.7 |
Fe(OH)2 | 7.6 | 9.6 |
Mg(OH)2 | 9.9 | 11.0 |
(1)写出“氧化”过程中发生的离子反应方程式_______________。
(2)pH调节的范围___________,滤渣的主要成分___________(填化学式)。
(3)操作X包括过滤、洗涤、烘干,证明碳酸镁晶须已经洗涤干净的方法______________。
(4)水浸后溶液中Fe2+、Fe3+含量的测定
①取水浸后溶液100.00 mL,测得Cl-的浓度为0.455 mol·L-1,向其中缓缓通入氯气使Fe2+恰好完全转化为Fe3+,测得此时溶液中Cl-的浓度为0.460 mol·L-1(溶液体积变化忽略不计)。
②另取水浸后溶液100.00 mL,向其中加入过量的1 mol·L-1NaOH溶液,充分反应后过滤、洗涤、灼烧,冷却后,称得固体粉末的质量为0.96 g。试通过计算确定水浸后溶液中Fe2+、Fe3+的物质的量浓度(写出计算过程)。 _______________________