题目内容
【题目】工业上用铝土矿![]() 主要成分为
主要成分为![]() ,还有少量的
,还有少量的![]() 等杂质
等杂质![]() 提取氧化铝作冶炼铝的原料,提取的操作过程如下:
提取氧化铝作冶炼铝的原料,提取的操作过程如下:
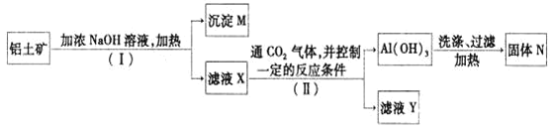
(1)![]() 和II步骤中分离溶液和沉淀的操作为_________,所用到的玻璃仪器是:________;
和II步骤中分离溶液和沉淀的操作为_________,所用到的玻璃仪器是:________;
(2)沉淀M中除含有泥沙外,一定还含有_______,固体N是_______;
(3)滤液X中,含铝元素的溶质的化学式为______,它属于_____![]() 填“酸”、“碱”或“盐”
填“酸”、“碱”或“盐”![]() 类物质;
类物质;
(4)实验室里常往![]() 溶液中加入___________
溶液中加入___________![]() 填“氨水”或“NaOH溶液”
填“氨水”或“NaOH溶液”![]() 来制取
来制取![]() ;
;
(5)将铝粉和氧化铁的混合物点燃,反应放出大量的热量,生成的液态的铁用来焊接铁轨。请写出反应的化学方程式:______________________________________。
【答案】过滤 烧杯、漏斗、玻璃棒 Fe2O3 Al2O3 NaAlO2 盐 氨水 ![]()
【解析】
铝土矿中加入浓NaOH溶液,![]() 和氢氧化钠不反应,氧化铝与NaOH反应生成NaAlO2,步骤I利用过滤除去
和氢氧化钠不反应,氧化铝与NaOH反应生成NaAlO2,步骤I利用过滤除去![]() ,沉淀M为氧化铁等不溶物,滤液X含有偏铝酸钠;步骤II通入二氧化碳将AlO2-转化为氢氧化铝沉淀,过滤得氢氧化铝,加热分解氢氧化铝得到氧化铝。
,沉淀M为氧化铁等不溶物,滤液X含有偏铝酸钠;步骤II通入二氧化碳将AlO2-转化为氢氧化铝沉淀,过滤得氢氧化铝,加热分解氢氧化铝得到氧化铝。
(1)I和II步骤分离固体与溶液的方法为过滤,所用的玻璃仪器为:烧杯、漏斗、玻璃棒;
故答案为:过滤;烧杯、漏斗、玻璃棒
(2)由工艺流程可知,沉淀M中还含有![]() ,固体N为
,固体N为![]() ,
,
故答案为:![]() ;
;![]() ;
;
(3)由工艺流程可知,滤液X中,含铝元素的溶质的化学式为:![]() ,NaAlO2属于盐,
,NaAlO2属于盐,
故答案为:![]() ;盐;
;盐;
(4)氢氧化铝溶于强碱,实验室通常用弱碱氨水与铝盐制备氢氧化铝沉淀,反应的方程式为![]()
故答案为:氨水;
(5)铝和氧化铁反应生成铁和氧化铝的方程式为:![]() ,
,
故答案为:![]() 。
。

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案
相关题目