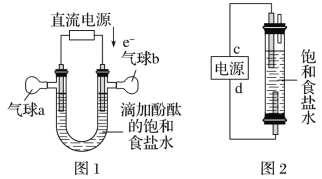
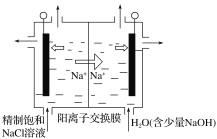
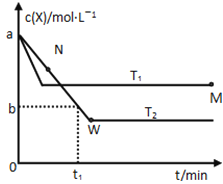
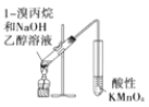
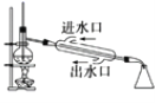
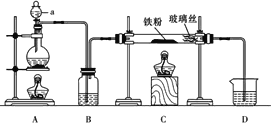
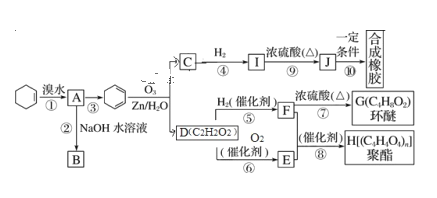
【题目】正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。

发生的反应如下:
CH3CH2CH2CH2OH![]() CH3CH2CH2CHO
CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
沸点/℃ | 密度/(g·cm-3) | 水中溶解性 | |
正丁醇 | 117.2 | 0.8109 | 微溶 |
正丁醛 | 75.7 | 0.8017 | 微溶 |
实验步骤如下:
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90—95℃,在E中收集90℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75—77℃馏分,产量2.0g。
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由_____。
(2)加入沸石的作用是_____。若加热后发现未加沸石,应采取的正确方法是______。
(3)上述装置图中,B仪器的名称是_____,D仪器的名称是_____。
(4)分液漏斗使用前必须进行的操作是_____(填正确答案标号)。
a.润湿 b.干燥 c.检漏 d.标定
(5)将正丁醛粗产品置于分液漏斗中分水时,水在_____层(填“上”或“下”)
(6)反应温度应保持在90—95℃,其原因是_____。
(7)本实验中,正丁醛的产率为_____%。
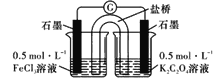
【题目】某学生欲用已知物质的量浓度的氢氧化钠来滴定测定未知物质的量浓度的盐酸溶液
(1)配制 500ml 浓度为 0.1 mol·L -1 的氢氧化钠溶液的操作步骤依次是:称量、____冷却并转移入容量瓶、洗涤并转___摇匀。
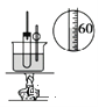
(2)用图中_____(填“甲”或“乙”)滴定管盛装 NaOH溶液。
![]()
(3)进行滴定操作时,该学生的实验步骤如下:
A.
B.用蒸馏水洗干净滴定管
C.碱式滴定管用标准液润洗后,将标准液注入碱式滴定管刻度“0”以上 2-3cm 处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下
D.用待测定的盐酸溶液润洗酸式滴定管
E.用酸式滴定管取待测HCl溶液25.00mL,注入锥形瓶中,加入2滴酚酞;
F.把锥形瓶放在滴定管下面,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度G.另取锥形瓶,再重复操作 2 次
上述步A的操作为____上述操作,如何判断滴定终点______
(4)下列操作中可能使所测盐酸溶液的浓度偏低的是_____
A.碱式滴定管未用标准氢氧化钠溶液润洗就直接注入标准液
B.滴定过程中,有液滴从锥形瓶中溅出
C.碱式滴定管在滴定前有气泡,滴定后气泡消失
D.读取氢氧化钠体积时,开始仰视读数,滴定结束时俯视读数
(5)某学生根据三次实验分别记录有关数据如下:请选用其中合理的数据计算该盐酸溶液的物质的量浓度:c(HCl) =_________
滴定次数 | 待测盐酸溶液的体积 /ml | 滴定前氢氧化钠的体积读数/ml | 滴定后氢氧化钠的体积读数/ml |
第一次 | 25.00 | 0.50 | 26.40 |
第二次 | 25.00 | 1.56 | 30.30 |
第三次 | 25.00 | 0.22 | 26.32 |