题目内容
【题目】下列实验装置能达到实验目的是(夹持仪器未画出)( )
A.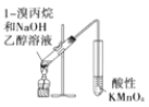 用于检验溴丙烷消去产物
用于检验溴丙烷消去产物
B.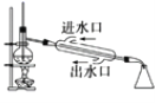 用于石油的分馏
用于石油的分馏
C.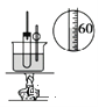 用于实验室制硝基苯
用于实验室制硝基苯
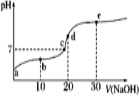
D.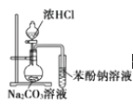 可证明酸性:盐酸>碳酸>苯酚
可证明酸性:盐酸>碳酸>苯酚
【答案】C
【解析】
A.1-溴丙烷在氢氧化钠乙醇溶液中共热发生消去反应生成丙烯,丙烯能被酸性高锰酸钾溶液氧化,使酸性高锰酸钾溶液褪色,而乙醇具有挥发性,挥发出的乙醇也能被酸性高锰酸钾溶液氧化,使酸性高锰酸钾溶液褪色,干扰烯烃的检验,则该实验不能说明烯烃的生成,故A错误;
B.由图可知,装置中温度计水银球的位置错误,分馏时应与蒸馏瓶支管下沿平齐测定馏出物的温度,冷凝管中冷凝水的流向错误,冷凝水应从下方进上方出,增强冷凝效果,故B错误;
C.实验室在浓硫酸作用下,苯和浓硝酸在50-60℃条件下发生硝化反应制硝基苯,实验时需要用水浴加热,故C正确;
D.盐酸的酸性强于碳酸,浓盐酸易挥发,挥发出的氯化氢可与苯酚钠反应制取苯酚,干扰碳酸和苯酚酸性的干扰,则该实验不能证明酸性碳酸>苯酚,故D错误;
故选C。

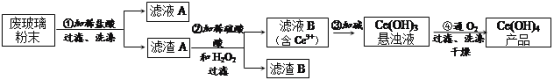
【题目】如图是从铝士矿(主要成分为Al2O3,还含有少量SiO2、Fe2O3等杂质)中提取Al2O3并生产AlN的工艺流程:

(1)“溶解”时,溶液中的硅酸钠与偏铝酸钠发生反应:2Na2SiO3+2NaAlO2+2H2O=Na2Al2Si2O8↓+4NaOH,赤泥的主要成分为_______(写出化学式)。
(2)“酸化”时通入过量CO2与NaAlO2反应生成Al(OH)3,滤液的主要成分为______(写出化学式)。 实验室过滤需用到的玻璃仪器有烧杯、__________、玻璃棒。
(3)“还原”时,炭黑在高温下被氧化为CO,反应的化学方程式为_______。
(4)现取三份不同质量的氮化铝样品(假设杂质只含有炭黑)分别加到20.00 mL相同浓度的NaOH溶液中,充分反应后,测得实验数据如下表所示。(已知:AlN+NaOH+H2O=NaAlO2+NH3↑)
实验序号 | I | II | III |
加入氮化铝样品的质量/g | 4.1 | 8.2 | 12.3 |
生成氨气的体积/L(标准状况) | 1.456 | 2.912 | 4.256 |
①该样品中AlN的质量分数为_____。
②所用NaOH溶液的浓度为___mol/L。