题目内容
【题目】下列说法正确的是
A.烷烃的通式为CnH2n+2,随n值增大,碳元素的质量百分含量逐渐减小
B.乙烯与溴水发生加成反应的产物为溴乙烷
C.1mol苯恰好与3mol氢气完全加成,说明一个苯分子中有三个碳碳双键
D.C7H16,主链上有5个碳原子的同分异构体共有5种
【答案】D
【解析】
A.烷烃的通式为CnH2n+2,C元素的质量分数为![]() ,则随n值增大,碳元素的质量百分含量逐渐增大,故A错误;
,则随n值增大,碳元素的质量百分含量逐渐增大,故A错误;
B.乙烯中含碳碳双键,可与溴水发生加成反应生成1,2-二溴乙烷,故B错误;
C.苯中不含碳碳双键,故C错误;
D.C7H16主链上有5个碳原子的烷烃,支链为2个甲基或1个乙基,符合的有(CH3)3CCH2CH2CH3、CH3CH2C(CH3)2CH2CH3、CH3CH2CH(CH2CH3)CH2CH3、(CH3)2CHCH2CH(CH3)2、(CH3)2CHCH(CH3)CH2CH3,共5种,故D正确;
答案选D。

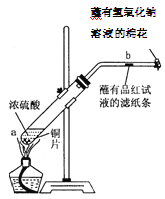
【题目】高铁酸盐在能源、环保等方面有着广泛的用途。利用湿法、干法制备高铁酸盐的原理如表所示。
湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
干法 | Fe2O3、KNO3、KOH混合加热生成紫红色高铁酸盐和KNO2等产物 |
(1)工业上利用湿法制备高铁酸钾(K2FeO4)的流程如图所示:
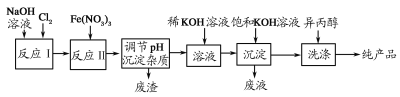
①反应Ⅰ的化学方程式为_____________。
②反应Ⅱ的离子方程式为_______________。
③加入饱和KOH溶液的目的_____________。
(2)高铁酸钾是一种理想的水处理剂,其处理水的原理为___________。
(3)干法制备K2FeO4的反应中,氧化剂是________。
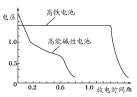
(4)高铁电池是正在研制中的可充电干电池,如图为该电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有________、________。