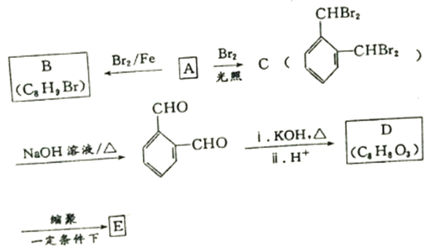
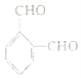
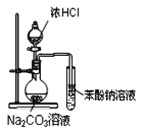
【题目】下列实验方案不能达到实验目的是
实验目的 | 实验方案 | |
A | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反产生的气体通入溴的四氯化碳溶液 |
B | 检验卤代烃中卤原子的种类 | 将溴乙烷与氢氧化钠溶液共热,取冷却后反应液,向其中滴加硝酸酸化后的硝酸银溶液 |
C | 检验 | 将 |
D | 验证苯和液溴在 | 将反应产生的混合气体先通入四氯化碳溶液再通入 |
A.AB.BC.CD.D
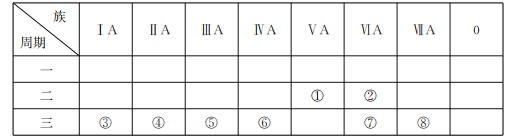
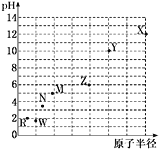
【题目】A、B、C、D、E是五种短周期主族元素。已知:
元素种类 | 性质 |
A | 短周期主族元素中原子半径最大 |
B | 最高价氧化物对应的水化物是一种两性氢氧化物 |
C | 热稳定性:HmD>HmC |
D | 质子数是A与B之和的 |
E | 原子序数最大的短周期主族元素 |
请回答下列问题:
(1)A元素在周期表中的位置为_____;Cm-的结构示意图为_____。
(2)五种元素的简单离子半径从大到小的顺序为_____(填离子符号)。
(3)A与D形成化合物的水溶液显强碱性,该水溶液不仅能溶解另外三种元素的单质,还能溶解一些化合物,请写出B2D3被溶解的离子方程式:____。
【题目】碳酸锶是重要的化工基础原料,由工业级硝酸锶(含有Ba2+、Ca2+、Mg2+等杂质)制备分析纯碳酸锶的工艺流程如下:
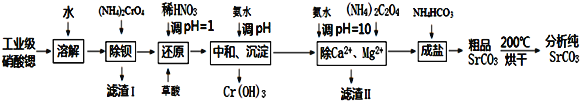
已知:①BaCrO4不溶于水,在水溶液中Cr2O72-与Ba2+不能结合。
②常温下,各物质的溶积常数如下表所示:
化合物 | Ca(OH)2 | CaC2O4 | Mg(OH)2 | MgC2O4 | Cr(OH)3 |
Ksp近似值 | 5.0×10-6 | 2.2×10-9 | 5.6×10-12 | 4.8×10-6 | 10-30 |
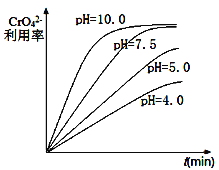
(1)“除钡”过程中CrO42-在不同pH时的利用率随时间变化曲线如下图所示,根据图像分析“除钡”过程中需要调节pH=7.5的原因_______________________________。
(2)“还原”过程中,应先调节pH=1.0,再加入草酸,加入草酸时发生反应的离子方程式为_____________________________。
(3)“滤渣Ⅱ”的主要成分为________________。
(4)“除Ca2+、Mg2+”后得到的滤液中除含有Sr(NO3)2外还含有过量的NH3·H2O,则“成盐”过程中发生反应的离子方程式为__________________________。
(5)“粗品SrCO3”烘干过程中除去的主要杂质为_____________________。
(6)在“中和、沉淀”步骤中,假定开始Cr3+,Zn3+浓度为0.1mol/L,调节至pH为_______时,铬开始沉淀;继续加碱调节至pH为_____时,铬刚好完全沉淀(离子浓度小于1×10-6mol/L时,即可认为该离子沉淀完全)。