【题目】汽车尾气污染是由汽车排放的废气造成的环境污染。主要污染物为一氧化碳、碳氢化合物、氮氧化合物等,对人类和动、植物危害甚大。解决汽车尾气问题的主要方法是研究高效催化剂促使尾气中的一氧化碳和氮氧化物反应,转化成无污染的氮气和二氧化碳。
回答下列问题:
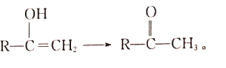
(1)在Co+的催化作用下,CO(g)还原N2O(g)的反应历程和能量变化如图所示(逸出后物质认为状态下发生变化,在图中略去)。已知总反应的化学方程式为:CO(g)+N2O(g)![]() CO2(g)+N2(g)。
CO2(g)+N2(g)。
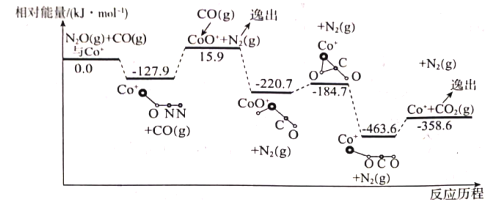
该反应分两步进行:
第一步:Co+(s)+N2O(g)![]() CoO+(s)+N2(g) △H1=+15.9kJmol-1;
CoO+(s)+N2(g) △H1=+15.9kJmol-1;
笫二步:___;△H2=___;
①填写第二步反应的热化学方程式,并根据反应历程图计算△H2的数值。
②该反应的最高能垒(活化能)为___。
(2)500℃条件下,在容积均为2L的三个密闭容器中,按不同方式投入反应物,发生上述反应,测得相关数据如下表:
容器 | 反应物投入的量 | 平衡时 n(N2/mol) | 达到平衡所需时间/min | 平衡时能量变化/kJ |
甲 | 1molCO和1molN2O | n1 | t1 | 放热Q1 |
乙 | 2molCO和2molN2O | n2 | t2 | 放热Q2 |
丙 | 2molCO2和2molN2 | n3 | t3 | 吸热Q3 |
①Q1+![]() ___358.6(填“>”“=”或“<”下同,t1___t2;
___358.6(填“>”“=”或“<”下同,t1___t2;
②500℃条件下,乙和丙两容器,气体混合物中N2O的物质的量分数x(N2O)与反应时间t的关系如下表:
t/s | 0 | 20 | 40 | 60 | 80 | 120 | |
乙 | x(N2O) | 0.5 | 0.32 | 0.20 | 0.12 | 0.088 | 0.07 |
丙 | x(N2O) | 0 | 0.030 | 0.048 | 0.059 | 0.065 | 0.07 |
根据上述实验结果,计算出乙容器中0~20s时间内的化学反应速率v(CO)=___;该反应的平衡常数K数值为:___;(保留3位有效数字)
③请推测并在图中画出甲容器中x(N2O)随时间变化的关系图象,标出恰好达到平衡时刻点的位置___。

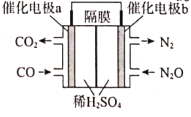
(3)若将CO(g)还原N2O(g)的反应设计成如图的原电池装置,则该电池正极的电极反应式为___。