��Ŀ����
����Ŀ������(COCl2)��ũҩ��ҽҩ���������ϵȷ��涼�й㷺Ӧ�ã�����������Ϊ��ɫ�����и���ζ������ʱΪ����ɫҺ�壬��ѧ���ʲ��ȶ�����ˮѸ��ˮ�⣬�����Ȼ��⡣ijʵ��С����������ʵ��װ�úϳɹ��������ù�����Ũ��ˮ��Ӧ�Ʊ�����[CO(NH2)2]����Ҫʵ��װ��(�г�װ����ȥ)�������������£�

�ٰ���ͼ����װ�ã�����װ�õ������ԣ�Ȼ���װʵ��ҩƷ��
�ڴ���a.����A�л���ͨ�������ȿ�����
��һ��ʱ���װ��D����Һ����ֲַ������һ��Һ�Ϸ��д�����ɫ������
��֪��3CC14+Al2O3=3COCl2+2AlC13
�ش��������⣺
(1)��������װ�õ������Եķ�����___��
(2)�������ͨ�������ȿ���������Ϊ___��
(3)װ��C������___��
(4)װ��D�з�Ӧ����������[CO(NH2)2���⣬����NH4Cl���ɣ��÷�Ӧ�Ļ�ѧ����ʽΪ___����
(5)����װ��D�л��Һ�IJ�������Ϊ___��
(6)װ��E��������NaOH��Һ�������Ĺ�����Ӧ�����ӷ���ʽΪ��___��
(7)ʵ���D����Һ�������ᾧ�������ؽᾧ�ķ����õ����ؾ���(����������NH4Cl����)���ⶨ���þ��������صİٷֺ����ķ�������7.07g��������������ȫת��Ϊ�������ð�����100mL2.00molL-1��������Һ��ȫ���գ�ȡ����Һ10mL��0.4000molL-1���������Ʊ���Һ�ζ���
�ٵ���ζ��յ�ʱ��������������45.00mL����þ��������ص���������Ϊ___(����3λ��Ч����)��
�����ζ�ǰδ���������Ʊ���Һ��ϴ�ζ��ܣ����ø��徧�����ص���������___(ѡ����ƫ��������ƫС��)��
���𰸡��رջ���a����װ��ĩ�˵��ܲ���ʢˮ���ձ��У�����װ��A���۲�ĩ�˵��ܿ������ݲ�����ֹͣ���ȣ�ĩ�˵��ܿ���һ��ˮ�� ��������CCl4�����ҽ��ȵ�CC14�������������Bװ�÷�����Ӧ ��ֹDװ���е�ˮ����װ��B�����¹�������ˮ�ⷴӦ COC12+4NH3H2O=CO(NH2)2+2NH4Cl+4H2O ��Һ COCl2+4OH-=CO32-+2Cl-+2H2O 84.9% ƫС
��������
��ʵ��Ŀ���Ǻϳɹ��������ù�����Ũ��ˮ��Ӧ�Ʊ�����[CO(NH2)2]��������ѧ���ʲ��ȶ�����ˮѸ��ˮ�⣬�����Ʊ�����ʱҪ������ϵ����ø�����ȿ����������������Ȼ�̼�������䴵��Bװ������Al2O3���з�Ӧ�Ʊ�������Cװ�ÿ��Է�ֹˮ��������Bװ�ã�����ͨ��Ũ��ˮ�з�Ӧ�Ʊ�[CO(NH2)2]��D���б������������Ȼ�̼���������Ȼ�̼������ˮ�����Գ��ֲַ�����δ��Ӧ�Ĺ����ڻ��Һ�Ϸ���ˮ������Ӧ����HCl��CO2��HCl�����ӷ����İ�����Ӧ�����Ȼ�泥����Բ����������̣�װ��E��������β����
(7)�ζ�ԭ��Ϊ�Ƚ���Ʒ�е�NԪ��ȫ��ת��Ϊ�������������գ�Ȼ����NaOH��Һ�ζ�ʣ�������������Ӷ�ȷ��NԪ�ص������ٸ����غ㷨����ȷ����Ʒ�����صĺ�����
(1)����ͨ�����ȷ�����װ�õ������ԣ��������Ϊ���رջ���a����װ��ĩ�˵��ܲ���ʢˮ���ձ��У�����װ��A���۲�ĩ�˵��ܿ������ݲ�����ֹͣ���ȣ�ĩ�˵��ܿ���һ��ˮ����˵�����������ã�
(2)���ݷ�����֪ͨ������ȿ���������Ϊ��������CCl4�����ҽ��ȵ�CC14�������������Bװ�÷�����Ӧ��
(3)������ѧ���ʲ��ȶ�����ˮѸ��ˮ�⣬װ��C��������Ҫ�Ƿ�ֹDװ���е�ˮ��������װ��B�����¹�������ˮ�ⷴӦ��
(4)D�з�Ӧ��ΪCOCl2��һˮ�ϰ���������[CO(NH2)2]��NH4Cl�ȣ�����Ԫ���غ�ɵ÷���ʽΪCOC12+4NH3H2O=CO(NH2)2+2NH4Cl+4H2O��
(5)װ��D����Һ�ֲ㣬��ͨ����Һ�ķ������룻
(6)������ˮˮ�����HCl��CO2��HCl��NaOH��Ӧ����NaCl��ˮ��CO2��NaOH��Ӧ����Na2CO3��ˮ�����Թ�����NaOH��Һ��Ӧ�����ӷ���ʽΪCOCl2+4OH-=CO32-+2Cl-+2H2O��
(7)�ٵ���ζ��յ�ʱ��������������45.00mL����10mL����Һʣ��n(H+)=0.045L��0.4000mol/L=0.018mol�������õİ���n(NH3)=0.1L��2.00mol/L��2-![]() =0.22mol���辧����n([CO(NH2)2])=x mol��n(NH4+)=y mol��
=0.22mol���辧����n([CO(NH2)2])=x mol��n(NH4+)=y mol��
����Ԫ���غ�ɵ�![]() �����x=0.1mol��y=0.02mol���������ص���������Ϊ
�����x=0.1mol��y=0.02mol���������ص���������Ϊ![]() ��100%=84.9%��
��100%=84.9%��
�����ζ�ǰδ���������Ʊ���Һ��ϴ�ζ���,��ʹ���ĵ��������Ʊ���Һƫ�࣬���øþ��������ص���������ƫС��

 �����ҵ���������ϵ�д�
�����ҵ���������ϵ�д� �����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д�
�����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д� �����ҵ�����������ѧ���ӳ�����ϵ�д�
�����ҵ�����������ѧ���ӳ�����ϵ�д�����Ŀ����ҵ����![]() �Ͱ�ˮ�Ļ��Һ��ȡ��ͭ�����еĵ���ͭ���õ�
�Ͱ�ˮ�Ļ��Һ��ȡ��ͭ�����еĵ���ͭ���õ�![]() ��ijС��ͬѧ��ͨ��ʵ��̽����ԭ����
��ijС��ͬѧ��ͨ��ʵ��̽����ԭ����
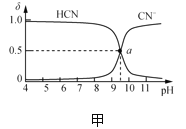
���������ϣ�i.![]() ������ɫ��
������ɫ��![]() �������ֽ⣬�ų�������
�������ֽ⣬�ų�������
ii.![]() ��ˮ��Һ�в��ȶ���
��ˮ��Һ�в��ȶ���![]() ����Һ��ֻ����
����Һ��ֻ����![]() ��������ӵ���ʽ�ȶ����ڣ�
��������ӵ���ʽ�ȶ����ڣ�![]() ��ɫ���ױ���������Ϊ
��ɫ���ױ���������Ϊ![]() ��
��
��ʵ��1���Ʊ�![]() ��
��
��ʢ��![]() ��Һ���Թ��еμ�
��Һ���Թ��еμ�![]() ��ˮ���۲쵽��Һ����������dz��ɫ���������������ܽ⣬�õ�����ɫ��Һ��������õ�
��ˮ���۲쵽��Һ����������dz��ɫ���������������ܽ⣬�õ�����ɫ��Һ��������õ�![]() ���塣
���塣
(1)���ϱ�������![]() ��Һ�еμӰ�ˮ�����ܻ�����dz��ɫ
��Һ�еμӰ�ˮ�����ܻ�����dz��ɫ![]() ������
������
�ٸ�С��ͬѧȡʵ��1��dz��ɫ������ϴ�Ӻ�____________(��ȫʵ�����������)��֤�������к���![]() ��
��
�ڲ�ȫʵ��1������![]() ���������ӷ���ʽ��
���������ӷ���ʽ��
![]() ____________+
____________+![]() ____________
____________
(2)��ͬѧ���ʵ��֤������ɫ��Һ�к�![]() ����������ɫ��Һ�������ݳ�����Ϊ����������Ϊ�˷���____________(����������������������)��������____________��
����������ɫ��Һ�������ݳ�����Ϊ����������Ϊ�˷���____________(����������������������)��������____________��
��ʵ��2��̽����![]() �Ͱ�ˮ�Ļ��Һ��ȡ����ͭ�õ�
�Ͱ�ˮ�Ļ��Һ��ȡ����ͭ�õ�![]() ��ԭ����
��ԭ����
��� | ʵ��װ�ü����ֲ��� | �ձ�����Һ | ʵ������ |
2-1 |
ʵ�鿪ʼ���ȶ�ȡ��ѹ��ʾ������Ѹ�ٽ��任�ɵ�����������ʵ�飬 10 min�ڼ�¼���ձ������� | �ף� �ң� | ��ѹ��ָ��Ѹ��ƫת��0.1V��������Һ�����Ա仯 |
2-2 | �ף� �ң� | ��ѹ��ָ��Ѹ��ƫת��0.3V��������Һ�����Ա仯 | |
2-3 | �ף� �ң���ҺA | ��ѹ��ָ��Ѹ��ƫת��0.35V��������Һ�����Ա仯 | |
2-4 | �ף� �ң� | ��ѹ��ָ��Ѹ�ٱ�ת��0.65V�������Ӻ��ձ���Һ������ɫ����ɫ |
��֪������������ͬʱ������ԭ��ط�Ӧ��������(��ԭ��)��������(��ԭ��)Խǿ�����ĵ�ѹԽ��
(3)��ҺAΪ____________��
(4)�Ա�ʵ��2-1��2-2�����Եõ�������____________��
(5)ʵ��2-4�У����ձ�����Һ����ɫ��Ϊ��ɫ��ԭ����____________��
(6)��������ʵ�飬������![]() �Ͱ�ˮ�Ļ��Һ��ȡ����ͭ��ԭ����____________��
�Ͱ�ˮ�Ļ��Һ��ȡ����ͭ��ԭ����____________��
����Ŀ�����������(��Ҫ����MoO3��NiO��MgO��Fe2O3)����ȡԪ�أ�����Ҫ��ҵ������ͼ��

��֪����MoO3������ˮ��������ǿ����Һ��
��Fe2O3��MgO������NH4Cl����ˮ���Һ��NiO������NH4Cl����ˮ���Һ����[Ni(NH3)6]2+��
����֪���ֽ��������γ��������������pH���±���
pH(��ʼ����) | pH(��ȫ����) | |
Fe3+ | 1.52 | 3.18 |
Mg2+ | 8.10 | 9.43 |
��ش��������⣺
(1)�������ʱӦ�Ƚ�����������飬����NaOH��80���·�Ӧ2Сʱ���ò�����Ŀ��Ϊ___��
(2)�������ʱ��MoO3������Ӧ�����ӷ���ʽΪ___��
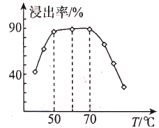
(3)�����ܽ�����Ŀ��Ϊ___�������ܽ��������з�Ӧ������ѡ����ʵ��������ͼ��ʾ�������ܽ�����������Ҫ�����¶���50~70��֮�䣬�¶ȹ�����Ͷ��ᵼ�²�Ʒ�IJ������ͣ������ԭ��___��
(4)��������������I���Ʊ�����������ķ�����___��
(5)��һ�γ�����ʱ����H2S��Ŀ���ǽ���Ԫ��ת��ΪNiS��������Ӧ�����ӷ���ʽΪ___��
(6)��������ʱ������Ӧ���������뻹ԭ�������ʵ���֮��Ϊ___��
(7)�����γ�����ʱ��������Ӧ�����ӷ���ʽΪ___��
(8)��֪��ij�¶�ʱ��Ksp(NiC2O4)=4.0��10-10��Ksp(NiCO3)=1.60��10-8�����¶��£���̼��������Ͷ�뵽1Lһ��Ũ�ȵ�Na2C2O4��Һ�У���Ҫһ����ǡ�ý�1molNiCO3��ȫת����NiC2O4��������Na2C2O4��Һ��Ũ��c(Na2C2O4)=___(������Һ����ı仯)��