9.常温时,将a1mL,b1mol/L 的CH3COOH溶液加入到a2mL,b2mol/L 的NaOH溶液中,下列结论中不正确的是( )
| A. | 如果a1b1=a2b2,则混合溶液的pH>7 | |
| B. | 如果混合液的pH=7,则混合溶液中c(CH3COO-)=c(Na+) | |
| C. | 如果a1=a2,b1=b2,则混合液液中c(CH3COO-)=c(Na+) | |
| D. | 如果a1=a2,且混合溶液的pH<7,则b1>b2 |
8.下列叙述正确的是( )
| A. | 同主族金属的原子半径越大,熔点越高 | |
| B. | 分子间作用力越强,分子晶体的熔点越高 | |
| C. | 稀有气体原子序数越大,熔点越低 | |
| D. | 同周期元素的原子半径越小,越易失去电子 |
6.有关煤的综合利用如图所示.下列说法正确的是( )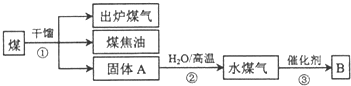

| A. | 煤和水煤气均是二次能源 | |
| B. | 煤中含有苯、甲苯、二甲苯等有机物 | |
| C. | ①是将煤在空气中加强热使其分解的过程 | |
| D. | B为甲醇或乙酸时,原子利用率均达到100% |
5.碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂.工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如图:
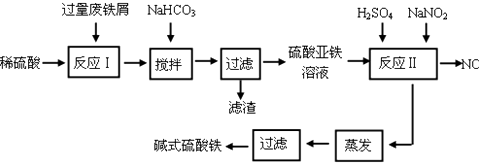
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
回答下列问题:
(1)如何加快废铁屑的溶解,写出两种办法搅拌、加热.
(2)加入少量NaHCO3的目的是调节pH在4.4-7.5范围内.
(3)反应Ⅱ中加入NaNO2的目的是将亚铁离子氧化为铁离子.
(4)碱式硫酸铁溶于水后生成的Fe(OH)2+离子可部分水解生成Fe2(OH)42+聚合离子,该水解反应的离子方程式为2Fe(OH)2++2H2O?Fe2(OH)42++2H+.
(5)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO3-.为检验所得产品中是否含有Fe2+,应使用的试剂为C.
A.氯水 B.KSCN溶液 C.酸性KMnO4溶液 D.NaOH溶液
(6)为测定含Fe2+和Fe3+溶液中铁元素的总含量,实验操作如下:准确量取20.00mL溶液于带塞锥形瓶中,加入足量H2O2,调节pH<2,加热除去过量H2O2;加入过量KI充分反应后,再用 0.1000mol/L Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL.
已知:2Fe3++2I-═2Fe2++I2 I2+2S2O32-═2I-+S4O62-
则溶液中铁元素的总含量为g/L.若滴定前溶液中H2O2没有除尽,所测定的铁元素的含量将会偏高 (填“偏高”“偏低”“不变”).

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)如何加快废铁屑的溶解,写出两种办法搅拌、加热.
(2)加入少量NaHCO3的目的是调节pH在4.4-7.5范围内.
(3)反应Ⅱ中加入NaNO2的目的是将亚铁离子氧化为铁离子.
(4)碱式硫酸铁溶于水后生成的Fe(OH)2+离子可部分水解生成Fe2(OH)42+聚合离子,该水解反应的离子方程式为2Fe(OH)2++2H2O?Fe2(OH)42++2H+.
(5)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO3-.为检验所得产品中是否含有Fe2+,应使用的试剂为C.
A.氯水 B.KSCN溶液 C.酸性KMnO4溶液 D.NaOH溶液
(6)为测定含Fe2+和Fe3+溶液中铁元素的总含量,实验操作如下:准确量取20.00mL溶液于带塞锥形瓶中,加入足量H2O2,调节pH<2,加热除去过量H2O2;加入过量KI充分反应后,再用 0.1000mol/L Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL.
已知:2Fe3++2I-═2Fe2++I2 I2+2S2O32-═2I-+S4O62-
则溶液中铁元素的总含量为g/L.若滴定前溶液中H2O2没有除尽,所测定的铁元素的含量将会偏高 (填“偏高”“偏低”“不变”).
3.下列说法正确的是( )
| A. | 碳元素的单质只存在金刚石和石墨两种同素异形体 | |
| B. | Mg、MgO中镁元素微粒的半径:r(Mg2+)>r(Mg) | |
| C. | 粗硅$→_{高温}^{Cl_{2}}$SiCl4$→_{高温}^{H_{2}}$Si | |
| D. | Mg(OH)2$\stackrel{盐酸}{→}$MgCl2(aq)$\stackrel{电解}{→}$Mg |
2.现有常温下的四种溶液:①pH=11的氨水、②0.001mol/L的NaOH溶液、③pH=3的醋酸、④由水电离出的c(H+)=10-11mol/L的盐酸.下列有关叙述正确的是( )
0 172783 172791 172797 172801 172807 172809 172813 172819 172821 172827 172833 172837 172839 172843 172849 172851 172857 172861 172863 172867 172869 172873 172875 172877 172878 172879 172881 172882 172883 172885 172887 172891 172893 172897 172899 172903 172909 172911 172917 172921 172923 172927 172933 172939 172941 172947 172951 172953 172959 172963 172969 172977 203614
| A. | 分别加水稀释10倍,四种溶液的pH:①>②>④>③ | |
| B. | 将③、④分别稀释到pH=5,由水电离出氢离子的浓度均减小100倍 | |
| C. | 在①、②中分别加入适量的氯化铵晶体后,①的pH减小,②的pH不变 | |
| D. | 将①、④两种溶液等体积混合,所得溶液中:c(OH-):c(H+)<1 |