20.下列物质均有漂白作用,其漂白原理相同的是( )
①二氧化硫
②次氯酸
③过氧化钠
④活性炭
⑤臭氧
⑥过氧化氢.
①二氧化硫
②次氯酸
③过氧化钠
④活性炭
⑤臭氧
⑥过氧化氢.
| A. | ①②⑤⑥ | B. | ①②③④ | C. | ②③⑤⑥ | D. | ①④ |
19.将氯气通入紫色石蕊试液中,出现的现象为( )
| A. | 溶液变红 | B. | 溶液变蓝 | C. | 先变红后褪色 | D. | 不变色 |
17.下列事实不能用勒夏特列原理解释的是( )
| A. | 开启啤酒瓶后,瓶中立刻泛起大量泡沫 | |
| B. | 将盛有二氧化氮和四氧化二氮混合气的密闭容器置于冷水中,混合气体颜色变浅 | |
| C. | 向氯水中加CaCO3后,溶液漂白性增强 | |
| D. | 由H2、I2蒸气、HI组成的平衡体系加压后颜色变深 |
16.下列说法不正确的是( )
| A. | 任何一种微观粒子的摩尔质量以g/moL为单位时,其数值与该种粒子的相对分子(或原子)质量相同 | |
| B. | 物质的量是含有一定粒子数目的粒子的集合体 | |
| C. | 阿伏加德罗常数个微粒数就是12g12C原子所含的碳原子数 | |
| D. | 物质的量就是物质的质量 |
13.下列有机物命名正确的是( )
| A. | 3,3-二甲基丁烷 | B. | 2,2-二甲基丁烷 | ||
| C. | 2-乙基丁烷 | D. | 2,3,3-三甲基丁烷 |
12.设NA表示阿伏伽德罗常数的值,下列说法不正确的是( )
0 172388 172396 172402 172406 172412 172414 172418 172424 172426 172432 172438 172442 172444 172448 172454 172456 172462 172466 172468 172472 172474 172478 172480 172482 172483 172484 172486 172487 172488 172490 172492 172496 172498 172502 172504 172508 172514 172516 172522 172526 172528 172532 172538 172544 172546 172552 172556 172558 172564 172568 172574 172582 203614
| A. | 常温常压下18g水中含有的原子总数为3NA, | |
| B. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| C. | 标准状况下2.24LH2O中所含电子数为NA | |
| D. | 常温常压下,1.7gH2O2中含有的电子数为0.9NA |
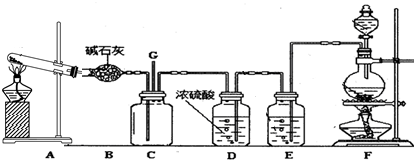
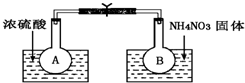 已知2NO2(g)═N2O4(g)△H(298K)=-52.7kJ•mol-1,某课外活动小组为了探究温度和压强对化学平衡的影响,做了如下两组实验:
已知2NO2(g)═N2O4(g)△H(298K)=-52.7kJ•mol-1,某课外活动小组为了探究温度和压强对化学平衡的影响,做了如下两组实验:



