题目内容
17.下列事实不能用勒夏特列原理解释的是( )| A. | 开启啤酒瓶后,瓶中立刻泛起大量泡沫 | |
| B. | 将盛有二氧化氮和四氧化二氮混合气的密闭容器置于冷水中,混合气体颜色变浅 | |
| C. | 向氯水中加CaCO3后,溶液漂白性增强 | |
| D. | 由H2、I2蒸气、HI组成的平衡体系加压后颜色变深 |
分析 勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动,使用勒夏特列原理时,该反应必须是可逆反应,否则勒夏特列原理不适用.
解答 解:A.开启啤酒瓶后,瓶中马上泛起大量泡沫,是压强对其影响导致的,属于可逆过程,可以用平衡移动原理解释,故A不选;
B.二氧化氮和四氧化二氮混合气体的密闭容器置于冷水中,化学平衡向着生成四氧化二氮的方向进行,颜色变浅,能用勒夏特利原理解释,故B不选;
C.依据氯水中的化学平衡为Cl2+H2O?HCl+HClO,加入碳酸钙和盐酸反应促进平衡正向进行,次氯酸浓度增大,漂白性增强,和平衡有关,能用勒夏特利原理解释,故C不选;
D.氢气与碘蒸气反应的平衡中,前后气体系数和是相等的,压强对平衡无影响,压缩气体,碘单质的浓度增大,颜色加深,不能用勒夏特利原理解释,故D选;
故选D.
点评 本题考查了勒夏特列原理的使用条件,难度不大,注意使用勒夏特列原理的前提必须是可逆反应.

练习册系列答案
相关题目
7.NA表示阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 1mol苯乙烯中含有的碳碳双键数为4NA | |
| B. | 7.8g过氧化钠晶体中含有0.1NA个O${\;}_{2}^{2-}$ | |
| C. | 标准状况下,22.4LNO2中含有NA个NO2分子 | |
| D. | 1mol•L-1NH4Cl溶液中,NH${\;}_{4}^{+}$的数目小于NA |
8.下列物质属于同系物的一组是( )
| A. | CH4与C2H4 | B. | C2H6与C3H8 | ||
| C. | 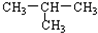 与CH3-CH2-CH2-CH3 与CH3-CH2-CH2-CH3 | D. | O2与O3 |
5.如图所示与对应的叙述相符的是( )
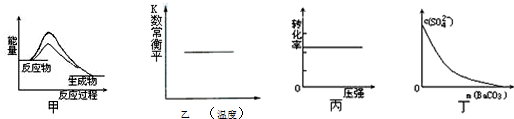

| A. | 图甲表示使用催化剂后,该反应的△H变小 | |
| B. | 图乙表示反应NO(g)+CO(g)?$\frac{1}{2}$N2(g)+CO2(g)△H=-373.4kJ•mol-1反应的平衡常数随温度的变化 | |
| C. | 图丙表示反应H2(g)+I2(g)?2HI(g)中H2的转化率随压强的变化 | |
| D. | 图丁表示在饱和Na2SO4溶液中逐步加BaCO3固体后,溶液中c(${SO}_{4}^{2-}$)的浓度变化 |
12.设NA表示阿伏伽德罗常数的值,下列说法不正确的是( )
| A. | 常温常压下18g水中含有的原子总数为3NA, | |
| B. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| C. | 标准状况下2.24LH2O中所含电子数为NA | |
| D. | 常温常压下,1.7gH2O2中含有的电子数为0.9NA |
2.下列关于有机物的说法正确的是( )
| A. | 实验室制备硝基苯加入试剂的顺序为:先加入浓硫酸,再滴加苯,最后滴加浓硝酸 | |
| B. | 蔗糖和葡萄糖不是同分异构体,但属同系物 | |
| C. | 可用金属钠区分乙酸、乙醇和苯 | |
| D. | 石油裂解和煤的干馏都是化学变化,而石油的分馏和煤的气化都是物理变化 |
6.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,2.24L氯气溶于水发生反应,转移的电子数目为0.1NA | |
| B. | 10g46%的乙醇水溶液中所含氢原子数目为0.06NA | |
| C. | 1L1 mol•L-1的NH4NO3溶液中含有NH4+数目为NA | |
| D. | 25℃时,100mlpH=13的Ba(OH)2溶液中OH-的数目为0.01NA |