7.下列各组离子在指定溶液中,一定能大量共存的是( )
| A. | 加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,SO42- | |
| B. | 含有NaClO的溶液中:K+,Al3+,Br-,S2- | |
| C. | 澄清透明溶液:Cu2+、SO42-、HCO3-、H+ | |
| D. | 使甲基橙变红的溶液中:Fe2+,MnO4-,Na+,SO42- |
6.由铝屑、盐酸、氢氧化钠溶液反应制取1mol Al(OH)3,至少需要消耗HCl和NaOH的物质的量为( )
| A. | 0.25mol,0.25mol | B. | 0.75mol,0.75mol | C. | 1mol,1mol | D. | 3mol,3mol |
5.下列有关化学反应速率的说法中,正确的是( )
| A. | 铁片与稀盐酸制取氢气时,加入NaNO3固体或Na2SO4固体都不影响生成氢气的速率 | |
| B. | 等质量的锌片分别与同体积、同物质的量浓度的盐酸、硫酸反应,反应速率不相等 | |
| C. | SO2的催化氧化是一个放热反应,所以升高温度,反应速率减慢 | |
| D. | 加入反应物,单位体积内活化分子百分数增大,化学反应速率增大 |
4.已知适当条件下+7、+6、+4价锰的化合物都能和浓盐酸反应制得氯气且还原产物都是MnCl2.将6.32g KMnO4粉末加热一段时间后收集到0.112L气体(标准状况,后同),冷却后放入足量的浓盐酸再加热,又收集到VL黄绿色气体,下列说法正确的是( )
| A. | V=2.24L | |
| B. | 参加反应的HCl为0.18mol | |
| C. | 无法确定最终生成含钾化合物的数量是多少 | |
| D. | 6.32g KMnO4粉末若直接与足量浓盐酸反应可得到2.24L Cl2 |
3.工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2.在该反应中( )
| A. | 二氧化硫体现还原性,做还原剂 | |
| B. | 氧化剂与还原剂的物质的量之比为1:2 | |
| C. | 每生成1molNa2S2O3,转移4mol电子 | |
| D. | 相同条件下,每吸收10m3SO2就会放出2.5m3CO2 |
2.下列反应中的氨与反应4NH3+5O2→4NO+6H2O中的氨作用相同的是( )
| A. | 2Na+2NH3→2NaNH2+H2↑ | B. | NH3+HNO3→NH4NO3 | ||
| C. | 4NH3+6NO→5N2+6H2O | D. | 3SiH4+4NH3→Si3N4+12H2 |
1.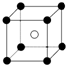 最近发现一种由M、N原子构成的两种原子的气态团簇分子,如图所示.实心球“●”表示N原子,空心球“○”表示M原子,它的化学式为( )
最近发现一种由M、N原子构成的两种原子的气态团簇分子,如图所示.实心球“●”表示N原子,空心球“○”表示M原子,它的化学式为( )
 最近发现一种由M、N原子构成的两种原子的气态团簇分子,如图所示.实心球“●”表示N原子,空心球“○”表示M原子,它的化学式为( )
最近发现一种由M、N原子构成的两种原子的气态团簇分子,如图所示.实心球“●”表示N原子,空心球“○”表示M原子,它的化学式为( )| A. | M4N4 | B. | MN8 | C. | MN | D. | M4N5 |
20.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
0 172352 172360 172366 172370 172376 172378 172382 172388 172390 172396 172402 172406 172408 172412 172418 172420 172426 172430 172432 172436 172438 172442 172444 172446 172447 172448 172450 172451 172452 172454 172456 172460 172462 172466 172468 172472 172478 172480 172486 172490 172492 172496 172502 172508 172510 172516 172520 172522 172528 172532 172538 172546 203614
| A. | 标准状况下,22.4LNO与CO2的混合气体中含有O原子数为3NA | |
| B. | 0.1mol NH3溶于足量水中(不考虑氨气挥发),溶液中N原子的数目为0.1NA | |
| C. | 0.1molN2与足量的H2反应,转移的电子数是0.6NA | |
| D. | 58.5 g的NaCl固体中含有NA个氯化钠分子 |
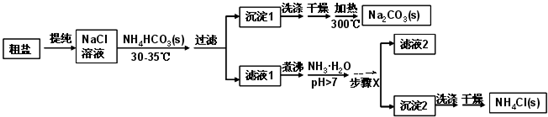
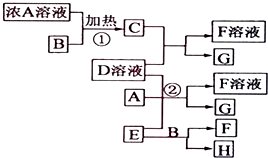 以下均为中学化学常见物质,存在如图转化关系(部分产物已省略).通常C为气体单质,G为紫黑色固体单质.实验室中,常用固体E在B的催化下加热制取气体单质H.
以下均为中学化学常见物质,存在如图转化关系(部分产物已省略).通常C为气体单质,G为紫黑色固体单质.实验室中,常用固体E在B的催化下加热制取气体单质H.