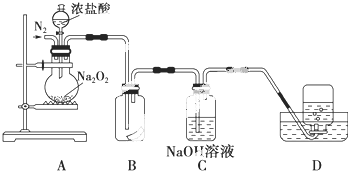
8.如表根据实验操作和现象所得出的结论错误的是( )
| 选 项 | 实验操作 | 实验现象 | 结论 |
| A | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有完全变质 |
| B | 将少量的溴水滴入FeCl2、NaI的混合溶液中,再滴加CCl4,振荡、静置,向上层溶液中滴加KSCN溶液.再向上层溶液中滴加溴水 | 实验现象1: 上层溶液不变红,下层溶液呈紫红色 实验现象2: 上层溶液变红 | 氧化性:Br2>Fe3+>I2 |
| C | 将一片铝箔置于酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面有致密Al2O3薄膜,且Al2O3熔点高于Al的 |
| D | 取久置的绿矾(FeSO4•7H2O)溶于水,加入KSCN溶液 | 溶液变为红色 | 绿矾部分或全部被氧化 |
| A. | A | B. | B | C. | C | D. | D |
4.Na2O2是一种既有氧化性、又有还原性的物质,当Na2O2与某物质Q发生反应并且有氧气生成时,下列有关说法正确的是( )
| A. | Q一定是氧化剂 | |
| B. | 当有1 mol O2生成时转移电子4 mol | |
| C. | O2一定是氧化产物 | |
| D. | Na2O2不可能发生还原反应 |
2.制取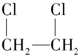 最合理的方法是( )
最合理的方法是( )
0 172348 172356 172362 172366 172372 172374 172378 172384 172386 172392 172398 172402 172404 172408 172414 172416 172422 172426 172428 172432 172434 172438 172440 172442 172443 172444 172446 172447 172448 172450 172452 172456 172458 172462 172464 172468 172474 172476 172482 172486 172488 172492 172498 172504 172506 172512 172516 172518 172524 172528 172534 172542 203614
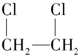 最合理的方法是( )
最合理的方法是( )| A. | CH3CH3与Cl2取代 | B. | CH2═CH2与HCl加成 | ||
| C. | CH2═CH2与Cl2加成 | D. | CH3CH2Cl与Cl2取代 |