9.2015年8月12日天津港瑞海公司危险化学品仓库发生特大火灾爆炸事故,事故警示我们,化学药品的安全存放是非常重要的.下列有关化学药品的存放说法不正确的是( )
| A. | 液溴易挥发,应用少量的水液封并放在冷暗处保存 | |
| B. | 硝酸见光易分解、易挥发,应用棕色广口试剂瓶密封保存 | |
| C. | 金属钠遇到氧气和水均立即反应,应保存在煤油中或者液体石蜡里 | |
| D. | 碳酸钠虽然属于盐,但是其水溶液呈碱性,应用带橡胶塞的试剂瓶保存 |
8.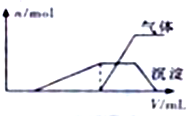 一份溶液中可能含有K+、Al3+、H+、NH4+、Cl-、Br-、I-、ClO-、AlO2- 等离子中的若干种.为了确定溶液的组成,进行了如下操作:
一份溶液中可能含有K+、Al3+、H+、NH4+、Cl-、Br-、I-、ClO-、AlO2- 等离子中的若干种.为了确定溶液的组成,进行了如下操作:
(1)往该溶液中逐滴加入NaOH溶液并适当加热,产生沉淀和气体的物质的量(n)与加
入NaOH溶液的体积关系如图所示;
则该溶液中一定存在的离子是Al3+、H+、NH4+,一定不存在的离子是ClO-、AlO2-.
(2)经检测后,该溶液中含有大量的Cl-、Br-、I-,若向1L该混合溶液中通入一定量的氯气,则溶液中Cl-、Br-、I-与通入氯气的体积(标况下)关系如图所示,回答下列问题:
①则a为0.15
②原溶液中Cl-、Br-、I-的物质的量浓度之比为10:15:4.
 一份溶液中可能含有K+、Al3+、H+、NH4+、Cl-、Br-、I-、ClO-、AlO2- 等离子中的若干种.为了确定溶液的组成,进行了如下操作:
一份溶液中可能含有K+、Al3+、H+、NH4+、Cl-、Br-、I-、ClO-、AlO2- 等离子中的若干种.为了确定溶液的组成,进行了如下操作:(1)往该溶液中逐滴加入NaOH溶液并适当加热,产生沉淀和气体的物质的量(n)与加
入NaOH溶液的体积关系如图所示;
则该溶液中一定存在的离子是Al3+、H+、NH4+,一定不存在的离子是ClO-、AlO2-.
(2)经检测后,该溶液中含有大量的Cl-、Br-、I-,若向1L该混合溶液中通入一定量的氯气,则溶液中Cl-、Br-、I-与通入氯气的体积(标况下)关系如图所示,回答下列问题:
| Cl2的体积(标况下) | 2.8L | 5.6L | 11.2L |
| n(Cl- ) | 1.25mol | 1.5mol | 2mol |
| n(Br- ) | 1.5mol | 1.4mol | 0.9mol |
| n(I- ) | a mol | 0 | 0 |
②原溶液中Cl-、Br-、I-的物质的量浓度之比为10:15:4.
7.下列离子方程式正确的是( )
| A. | 碳酸氢钠溶液与少量石灰水反应:HCO3-+OH-+Ca2+═H2O+CaCO3↓ | |
| B. | 氯化铵与氢氧化钠溶液混合:NH4++OH-═H2O+NH3↑ | |
| C. | 向漂白粉溶于水形成的溶液中通入少量的SO2:Ca2++3ClO-+SO2+H2O═CaSO4↓+Cl-+2HClO | |
| D. | 硫化亚铁溶于稀硝酸中:FeS+2H+═Fe2++H2S↑ |
6.实验是解决化学问题的基本途径,下列有关实验的叙述不正确的是( )
| A. | 240 mL 0.2 mol•L-1的NaOH溶液配制:需要使用天平、烧杯、250 mL容量瓶等仪器 | |
| B. | 除去Cu粉中的CuO,可向混合物中滴加适量稀硫酸再过滤 | |
| C. | 为增强氯水的漂白性,向其中加入碳酸钙 | |
| D. | 为使0.5mol/L的NaNO3溶液物质的量浓度变为1mol/L,可将原溶液加热蒸发掉50克水 |
5.在氢硫酸溶液中,通入或加入少量的下列物质:①O2;②Cl2;③SO2;④CuSO4;⑤NH3能使溶液的导电能力增强的是( )
| A. | ①②③ | B. | ②④⑤ | C. | ①④⑤ | D. | ②③④ |
4.固体NH5属离子化合物.它与水反应的方程式为:NH5+H2O═NH3•H2O+H2↑,它也能跟乙醇发生类似的反应,并都产生氢气.下列有关NH5叙述正确的是( )
| A. | 1mol NH5中含有5NA个N-H键 | |
| B. | NH5中N元素的化合价为-5价 | |
| C. | 与水反应时,原理和NaH与水反应相同 | |
| D. | 与乙醇反应时,NH5被还原 |
3.下列离子方程式中,正确的是( )
| A. | 碳酸氢钠与硫酸氢钠反应:HCO3-+HSO4-═SO42-+H2O+CO2↑ | |
| B. | 硫酸与氢氧化钡反应:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| C. | 锌和稀硫酸反应:Zn+2H+═Zn2++H2↑ | |
| D. | 氧化铜和盐酸反应:O2-+2H+═H2O |
2.下列反应的离子方程式正确的是( )
| A. | 碳酸钙与稀硝酸反应:CO32-+2H+═CO2↑+H2O | |
| B. | 铜与硝酸银溶液反应:Cu+2Ag+═2Ag+Cu2+ | |
| C. | 铁溶于稀硫酸中:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 氢氧化钡溶液中滴加稀硫酸:Ba2++SO42-═BaSO4↓ |
1.下列说法中正确的是( )
| A. | 摩尔既是物质的量的单位又是物质的质量单位 | |
| B. | 物质的量既表示物质的数量又表示物质的质量 | |
| C. | 阿伏加德罗常数是12kg碳12中含有的碳原子数目 | |
| D. | 1molH2O中含有10mol电子 |
20.1molC2H4和Cl2完全加成,再与Cl2光照条件下发生取代反应,所有氢原子被氯原子取代,则共消耗Cl2的物质的量是( )
0 172313 172321 172327 172331 172337 172339 172343 172349 172351 172357 172363 172367 172369 172373 172379 172381 172387 172391 172393 172397 172399 172403 172405 172407 172408 172409 172411 172412 172413 172415 172417 172421 172423 172427 172429 172433 172439 172441 172447 172451 172453 172457 172463 172469 172471 172477 172481 172483 172489 172493 172499 172507 203614
| A. | 6mol | B. | 5mol | C. | 4mol | D. | 3mol |