1.乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应、装置示意图1和有关数据如下:
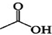 +
+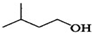 $?_{△}^{浓H_{2}SO_{4}}$
$?_{△}^{浓H_{2}SO_{4}}$ +H2O
+H2O
实验步骤:
在A中加入4.4g的异戊醇、6.0g的乙酸、数滴浓硫酸和2~3片碎瓷片.开始缓慢加热A,回流50min.反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g.
回答下列问题:
(1)仪器B的名称是球形冷凝管.
(2)在洗涤、分液操作中,应充分振荡,然后静置,待分层后d(填标号).
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(3)本实验中加入过量乙酸的目的是提高醇的转化率.
(4)实验中加入少量无水MgSO4的目的是干燥乙酸异戊酯.
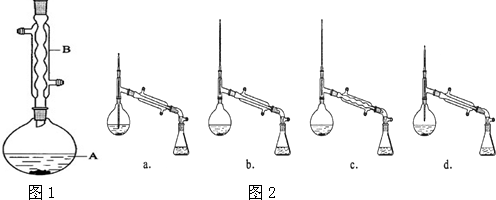
(5)在蒸馏操作中,图2中仪器选择及安装都正确的是b(填标号).
(6)在进行蒸馏操作时,若从130℃便开始收集馏分,会使实验的产率偏高(填“高”或“低”),原因是会收集少量未反应的异戊醇.
(7)本实验的产率是c(填标号).a.30% b.40% c.60% d.90%
 +
+ $?_{△}^{浓H_{2}SO_{4}}$
$?_{△}^{浓H_{2}SO_{4}}$ +H2O
+H2O| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
在A中加入4.4g的异戊醇、6.0g的乙酸、数滴浓硫酸和2~3片碎瓷片.开始缓慢加热A,回流50min.反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g.
回答下列问题:
(1)仪器B的名称是球形冷凝管.
(2)在洗涤、分液操作中,应充分振荡,然后静置,待分层后d(填标号).
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(3)本实验中加入过量乙酸的目的是提高醇的转化率.
(4)实验中加入少量无水MgSO4的目的是干燥乙酸异戊酯.
(5)在蒸馏操作中,图2中仪器选择及安装都正确的是b(填标号).

(6)在进行蒸馏操作时,若从130℃便开始收集馏分,会使实验的产率偏高(填“高”或“低”),原因是会收集少量未反应的异戊醇.
(7)本实验的产率是c(填标号).a.30% b.40% c.60% d.90%
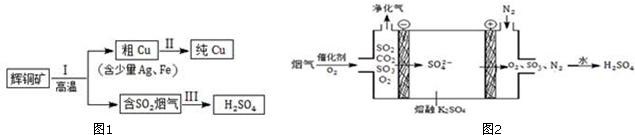
20.如图是利用废铜屑(含杂质铁)制备胆矾(硫酸铜晶体)的流程.
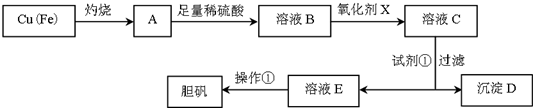
已知:
请回答:
(1)溶液B中含有的阳离子有Fe2+、Fe3+、H+、Cu2+(填离子符号).
(2)下列物质中最适宜作氧化剂X的是b(填字母).a.NaClO b.H2O2 c.KMnO4
(3)加入试剂①是为了调节pH,试剂①可以选择CuO或CuCO3或Cu(OH)2(填化学式).
(4)操作①的名称是蒸发浓缩、冷却结晶.
(5)沉淀D加入盐酸可以得到FeCl3,关于FeCl3溶液的性质中说法不正确的是c
a.将FeCl3饱和溶液逐滴加入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔效应
b.向FeCl3溶液滴加NaOH溶液,出现红褐色沉淀
c.将FeCl3溶液加热蒸干并灼烧,得到FeCl3固体
d.向FeCl3溶液中滴加KSCN溶液,溶液变为红色
(6)沉淀D加入盐酸和铁粉,可以制得FeCl2溶液.实验室保存FeCl2溶液,需加入过量的铁粉,其原因是2Fe3++Fe=3Fe2+(用离子方程式表示).

已知:
| 溶液中被沉淀离子 | Fe3+ | Fe2+ | Cu2+ |
| 完全生成氢氧化物沉淀时,溶液的pH | ≥3.7 | ≥6.4 | ≥4.4 |
(1)溶液B中含有的阳离子有Fe2+、Fe3+、H+、Cu2+(填离子符号).
(2)下列物质中最适宜作氧化剂X的是b(填字母).a.NaClO b.H2O2 c.KMnO4
(3)加入试剂①是为了调节pH,试剂①可以选择CuO或CuCO3或Cu(OH)2(填化学式).
(4)操作①的名称是蒸发浓缩、冷却结晶.
(5)沉淀D加入盐酸可以得到FeCl3,关于FeCl3溶液的性质中说法不正确的是c
a.将FeCl3饱和溶液逐滴加入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔效应
b.向FeCl3溶液滴加NaOH溶液,出现红褐色沉淀
c.将FeCl3溶液加热蒸干并灼烧,得到FeCl3固体
d.向FeCl3溶液中滴加KSCN溶液,溶液变为红色
(6)沉淀D加入盐酸和铁粉,可以制得FeCl2溶液.实验室保存FeCl2溶液,需加入过量的铁粉,其原因是2Fe3++Fe=3Fe2+(用离子方程式表示).
15. 已知25℃时部分弱电解质的电离平衡常数数据如表所示:
已知25℃时部分弱电解质的电离平衡常数数据如表所示:
回答下列问题:
(1)物质的量浓度均为0.1mol•L-1的三种溶液:a.CH3COONa b.Na2CO3 c.NaClO
pH由小到大排列的顺序是a<c<b(用编号填写).
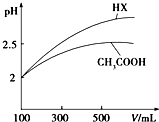
(2)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数大于(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数.稀释后,HX溶液中水电离出来的C(H+)大于(填“大于”、“小于”或“等于”)醋酸溶液中水电离出来的C(H+).
 已知25℃时部分弱电解质的电离平衡常数数据如表所示:
已知25℃时部分弱电解质的电离平衡常数数据如表所示:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Kal=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
(1)物质的量浓度均为0.1mol•L-1的三种溶液:a.CH3COONa b.Na2CO3 c.NaClO
pH由小到大排列的顺序是a<c<b(用编号填写).
(2)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数大于(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数.稀释后,HX溶液中水电离出来的C(H+)大于(填“大于”、“小于”或“等于”)醋酸溶液中水电离出来的C(H+).
13.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
0 172229 172237 172243 172247 172253 172255 172259 172265 172267 172273 172279 172283 172285 172289 172295 172297 172303 172307 172309 172313 172315 172319 172321 172323 172324 172325 172327 172328 172329 172331 172333 172337 172339 172343 172345 172349 172355 172357 172363 172367 172369 172373 172379 172385 172387 172393 172397 172399 172405 172409 172415 172423 203614
| A. | 18 g H2O含有10NA个质子 | |
| B. | 1 mol/LCH3COONa溶液中含有1 mol/LCH3COO- | |
| C. | 标准状况下,22.4 L氨水含有NA个NH3分子 | |
| D. | 56 g铁片投入足量浓H2SO4中生成NA个SO2分子 |

 $\stackrel{过氧化物}{→}$
$\stackrel{过氧化物}{→}$ (R,R′代表烃基)
(R,R′代表烃基) .
. .
.
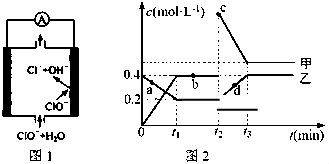
 氯元素是生产生活中常见的非金属元素
氯元素是生产生活中常见的非金属元素
 .
.
 .
.