16.下列溶液中微粒浓度关系一定正确的是( )
| A. | 将水加热到100℃,pH=6:c(H+)>c(OH-) | |
| B. | 0.1mol•L-1 的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+) | |
| C. | 室温下,pH=7的醋酸和醋酸钠的混合溶液中:c(CH3COO-)>c(Na+) | |
| D. | 同浓度的三种溶液:①CH3COONH4②NH4Cl③NH3•H2O中,c(NH4+)由大到小的顺序是②③① |
15.关于化学键的下列叙述中,正确的是( )
| A. | 离子化合物中不可能含共价键 | B. | 共价化合物中可能含离子键 | ||
| C. | 离子化合物中只含离子键 | D. | 共价化合物中不含离子键 |
14.下列物质中含离子键的是( )
| A. | HCl | B. | CH4 | C. | NaH | D. | NH3 |
13.下列式子书写正确的是( )
| A. | 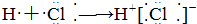 | B. | 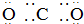 | ||
| C. | 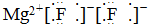 | D. |  |
12.某元素的一种同位素AY,其中子数为N,它与1H原子组成HmY分子,则在b g HmY分子中所含质子的物质的量( )
| A. | ($\frac{b}{A}$)(A-N)mol | B. | ($\frac{b}{A}$)(A-N+m)mol | C. | $\frac{b}{A+m}$(A-N)mol | D. | $\frac{b}{A+m}$(A-N+m)mol |
11.用NA表示阿伏加德罗常数的值.下列说法中正确的是( )
| A. | 2.4 g金属镁变成镁离子时失去的电子数为0.1NA | |
| B. | 2 g氢气中含有的原子数为NA | |
| C. | 3.01×1023个氮气分子中含有的原子数为2NA | |
| D. | 17g氨气中含有的电子数为10NA |
10.W、X、Y、Z四种元素均为短周期元素且原子序数依次增大,其简单离子都能促进水的电离的是( )
| A. | W2-、X+ | B. | X+、Y3+ | C. | X+、Z2- | D. | Y3+、Z2- |
9.常温下,有①氨水、②NH4Cl溶液、③Na2CO3溶液、④NaHCO3溶液各25mL,物质的量浓度均为0.1mol•L-1,下列说法正确的是( )
| A. | 四种溶液的pH的大小顺序:①>④>③>② | |
| B. | 将溶液①、②等体积混合所得碱性溶液中:c(NH4+)<c(NH3•H2O) | |
| C. | 向溶液①、②中分别滴加25mL 0.1mol•L-1盐酸后,溶液中c(NH4+):①>② | |
| D. | 将溶液③、④等体积混合所得溶液中:2c(OH-)-2c(H+)=3c(H2CO3)+c(HCO3-)-c(CO32-) |
8.25℃时,下列各溶液中,离子的物质的量浓度关系正确的是( )
| A. | 饱和氯化钾溶液中:c(K+)+c(H+)=c(Cl-)+c(OH-) | |
| B. | pH=11的氨水中:c(OH-)=3.0mol•L-1 | |
| C. | 饱和苏打溶液中:c(Na+)=c(CO32-) | |
| D. | pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol•L-1 |
7.下列措施合理的是( )
0 171844 171852 171858 171862 171868 171870 171874 171880 171882 171888 171894 171898 171900 171904 171910 171912 171918 171922 171924 171928 171930 171934 171936 171938 171939 171940 171942 171943 171944 171946 171948 171952 171954 171958 171960 171964 171970 171972 171978 171982 171984 171988 171994 172000 172002 172008 172012 172014 172020 172024 172030 172038 203614
| A. | 钢铁设备上连接铜块可以防止钢铁腐蚀 | |
| B. | 石英容器可盛放任何酸 | |
| C. | 生活中使用明矾净水,除去水中的悬浮的微小颗粒 | |
| D. | 向NaOH溶液中滴加FeCl3溶液制备Fe(OH)3胶体 |