题目内容
13.下列式子书写正确的是( )| A. | 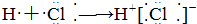 | B. | 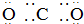 | ||
| C. | 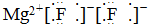 | D. |  |
分析 A、HCl是共价化合物;
B、CO2是共价化合物,其结构式为O=C=O,碳原子和氧原子之间有2对电子;
C、相同离子不能合并;
D、相同离子不能合并.
解答 解:A、HCl属于共价化合物,氢原子最外层电子与Cl最外层电子形成一对共用电子对,其形成过程为 ,故A错误;
,故A错误;
B、CO2是共价化合物,其结构式为O=C=O,碳原子和氧原子之间有2对电子,其电子式为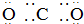 ,故B正确;
,故B正确;
C、镁原子失去2个电子形成镁离子,氟原子得到1个电子形成氟离子,1个镁离子与2个氟离子通过离子键结合形成氟化镁,电子式为: ,故C错误;
,故C错误;
D、Na2S为离子化合物,钠离子用离子符号表示,硫离子标出最外层电子,硫化钠的电子式为: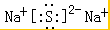 ,故D错误.
,故D错误.
故选B.
点评 本题考查电子式的书写,题目难度不大,注意掌握电子式的书写方法:简单阳离子的电子式为其离子符合,复杂的阳离子电子式除应标出共用电子对、非共用电子对等外,还应加中括号,并在括号的右上方标出离子所带的电荷.无论是简单阴离子,还是复杂的阴离子,都应标出电子对等,还应加中括号,并在括号的右上方标出离子所带的电荷.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.已知反应:①101kPa时,2C(s)+O2(g)═2CO(g);△H=-221kJ/mol
②稀溶液中,H+(aq)+OHˉ(aq)═H2O(l);△H=-57.3kJ/mol.下列结论正确的是( )
②稀溶液中,H+(aq)+OHˉ(aq)═H2O(l);△H=-57.3kJ/mol.下列结论正确的是( )
| A. | 碳的燃烧热小于110.5 kJ/mol | |
| B. | ①的反应热为221 kJ/mol | |
| C. | 稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水,放出的热量小于57.3 kJ |
4.把铁片放入下列溶液中,铁片溶解,溶液质量增加,但没有气体放出的是( )
| A. | 稀硫酸 | B. | Fe(NO3)3溶液 | C. | CuSO4溶液 | D. | AgNO3溶液 |
1.下列措施不合理的是( )
| A. | 用CCl4萃取碘水中的碘 | |
| B. | 将饱和FeCl3溶液滴入沸水中制备Fe(OH)3胶体 | |
| C. | 将混有少量HCl的Cl2通入饱和食盐水溶液中除去HCl | |
| D. | 常温下铝箔放在浓HNO3中,生成H2 |
8.25℃时,下列各溶液中,离子的物质的量浓度关系正确的是( )
| A. | 饱和氯化钾溶液中:c(K+)+c(H+)=c(Cl-)+c(OH-) | |
| B. | pH=11的氨水中:c(OH-)=3.0mol•L-1 | |
| C. | 饱和苏打溶液中:c(Na+)=c(CO32-) | |
| D. | pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol•L-1 |
18.下列物质属于强电解质的是( )
| A. | 盐酸 | B. | HF | C. | BaSO4 | D. | Cu |
2.下列叙述中正确的是( )
| A. | 常温常压下含有NA个原子的氦气体积约为22.4L | |
| B. | 常温常压下,O2和O3的混合物16g中约含有6.02×1023个氧原子 | |
| C. | 在0℃,101KPa时,22.4L氢气中含有NA个氢原子 | |
| D. | 标准状况下,33.6LH2O含有1.5NA个H2O分子 |
1.120℃、101kPa时,由两种烃组成的混合气体0.5L在4.5L O2中完全燃烧,测得反应后气体总体积小于5L,其中含CO2 0.8L,则生成水蒸气的体积为( )
| A. | 0.7L | B. | 1.0L | C. | 1.6L | D. | 2.5L |