题目内容
15.关于化学键的下列叙述中,正确的是( )| A. | 离子化合物中不可能含共价键 | B. | 共价化合物中可能含离子键 | ||
| C. | 离子化合物中只含离子键 | D. | 共价化合物中不含离子键 |
分析 共价键是有非金属原子之间通过共用电子对形成的化学键,既可存在于离子化合物中,也可存在于共价化合物中,离子键是离子之间的静电作用,只存在于离子化合物中,由此分析解答.
解答 解:A.离子化合物可能含共价键,如NaOH,故A错误;
B.共价化合物只含有共价键,故B错误;
C.离子化合物一定含有离子键,可能含有共价键,如NaOH,故C错误;
D.共价化合物只含有共价键,不含离子键,故D正确.
故选D.
点评 本题考查共价键、离子键以及共价化合物与离子化合物的区别,题目难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
5.已知:氨水的密度为0.990g/cm3时,NH3的质量分数为20%;氨水的密度为0.930g/cm3时,NH3的质量分数为18%.质量分数分别为a%和5a%的氨水按等体积混合均匀后,混合溶液中NH3的质量分数为( )
| A. | 3a% | B. | 6a% | C. | 大于3a% | D. | 小于3a% |
6.下列离子方程式正确的是( )
| A. | 碳酸氢钙溶液与盐酸混合:HCO3-+H+=H2O+CO2↑ | |
| B. | 氢氧化铜中加入盐酸:H++OH-=H2O | |
| C. | 氯化铁溶液中加入氢氧化钠溶液:Fe2++2OH-=Fe(OH)2↓ | |
| D. | 铁与盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
10.W、X、Y、Z四种元素均为短周期元素且原子序数依次增大,其简单离子都能促进水的电离的是( )
| A. | W2-、X+ | B. | X+、Y3+ | C. | X+、Z2- | D. | Y3+、Z2- |
20.火箭发射时可用肼(N2H4)为燃料和NO2作氧化剂,这两者反应生成氮气和水蒸气.已知:
N2(g)+2O2(g)=2NO2(g)△H=+67.7KJ/mol
N2H4(g)+O2(g)=N2 (g)+2H2O(g)△H=-534KJ/mol
则1摩尔气体肼和NO2完全反应时放出的热量为( )
N2(g)+2O2(g)=2NO2(g)△H=+67.7KJ/mol
N2H4(g)+O2(g)=N2 (g)+2H2O(g)△H=-534KJ/mol
则1摩尔气体肼和NO2完全反应时放出的热量为( )
| A. | 100.3KJ | B. | 567.85KJ | C. | 500.15KJ | D. | 601.7KJ |
7.对于相同质量的CO和CO2,下列关系正确的是( )
| A. | 所含氧原子的个数之比为1:2 | B. | 所含碳元素的质量之比为7:11 | ||
| C. | 所含氧元素的质量之比为11:14 | D. | 所含碳原子的个数之比为1:1 |
3.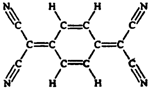 目前,世界上已合成了几百种有机超导体,TCNQ是其中之一.TCNQ的分子结构如图所示.下列关于TCNQ说法错误的是( )
目前,世界上已合成了几百种有机超导体,TCNQ是其中之一.TCNQ的分子结构如图所示.下列关于TCNQ说法错误的是( )
 目前,世界上已合成了几百种有机超导体,TCNQ是其中之一.TCNQ的分子结构如图所示.下列关于TCNQ说法错误的是( )
目前,世界上已合成了几百种有机超导体,TCNQ是其中之一.TCNQ的分子结构如图所示.下列关于TCNQ说法错误的是( )| A. | 该物质化学性质活泼,易氧化易加成 | |
| B. | 该分子不是平面分子,不可能所有原子共面 | |
| C. | 分子式为C12H4N4 | |
| D. | 该物质难溶于水 |