题目内容
12.某元素的一种同位素AY,其中子数为N,它与1H原子组成HmY分子,则在b g HmY分子中所含质子的物质的量( )| A. | ($\frac{b}{A}$)(A-N)mol | B. | ($\frac{b}{A}$)(A-N+m)mol | C. | $\frac{b}{A+m}$(A-N)mol | D. | $\frac{b}{A+m}$(A-N+m)mol |
分析 根据质子数=质量数-中子数,计算X原子质子数,进而计算每个HmX分子含有质子子数,根据n=$\frac{m}{M}$计算HmX的物质的量,结合每个分子含有质子数计算.
解答 解:某元素的一种同位素X的原子质量数为A,含N个中子,则质子数为(A-N),则每个HmX分子含有质子数为(A-N+m),bg HmX的物质的量为$\frac{bg}{(A+m)g/mol}$=$\frac{b}{A+m}$mol,故含有质子的物质的量为$\frac{b}{A+m}$×(A-N+m)mol;
故选D.
点评 本题考查物质的量有关计算、原子结构,比较基础,属于字母型计算,一定程度上增大计算难度

练习册系列答案
 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案
相关题目
20.设阿伏加德罗常数的数值为NA,下列说法正确的是( )
| A. | 常温常压下,16gO2含有的核外电子数为8 NA | |
| B. | 一定条件下,0.1mol铁与0.1mol Cl2充分反应,转移的电子数约为0.3 NA | |
| C. | 标准状况下,22.4L氨水含有NA个NH3分子 | |
| D. | 28gC2H4中含有C-H键的数目为3 NA |
7.下列措施合理的是( )
| A. | 钢铁设备上连接铜块可以防止钢铁腐蚀 | |
| B. | 石英容器可盛放任何酸 | |
| C. | 生活中使用明矾净水,除去水中的悬浮的微小颗粒 | |
| D. | 向NaOH溶液中滴加FeCl3溶液制备Fe(OH)3胶体 |
17.下列说法不正确的是( )
| A. | 加热可鉴别碳酸氢钠与碳酸钠 | |
| B. | 焰色反应可鉴别钾盐和钠盐 | |
| C. | 用水可鉴别氢氧化镁和氢氧化铝固体 | |
| D. | KSCN溶液可鉴别Fe3+与Fe2+ |
1.下列电离方程式正确的是( )
| A. | CaCl2=Ca2++Cl2? | B. | Na2SO4=Na++SO42- | ||
| C. | HNO3=H++NO3- | D. | NaHCO3=Na++H++CO32- |
20.第114号元素是化学家和物理学家很感兴趣的尚未发现的元素,推测此元素在周期表中的位置( )
| A. | 第八周期ⅢA族 | B. | 第六周期ⅤA族 | C. | 第七周期ⅣB族 | D. | 第七周期ⅣA族 |
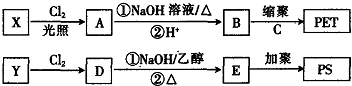
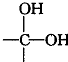 →
→
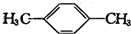 ,其核磁共振氢谱有2种峰.
,其核磁共振氢谱有2种峰. ,
, .
.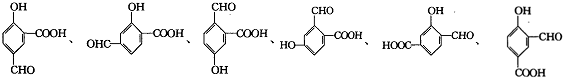 (其中一种).
(其中一种). $→_{②Zn/H_{2}O}^{①O_{3}}$R-CHO+
$→_{②Zn/H_{2}O}^{①O_{3}}$R-CHO+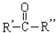
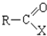 +H2O→R-COOH+HX
+H2O→R-COOH+HX
 、
、 ;
; +nH2O.
+nH2O.