5.在一定条件下,将钠与氧气反应的生成物1.5g溶于水,所得溶液恰好能被50g质量分数为2.92%的盐酸中和.则该生成物的成分是( )
| A. | Na2O | B. | Na2O2 | C. | Na2O和Na2O2 | D. | 不能确定 |
2.如图是实验室制备氯气并进行一系列相关实验的装置(部分夹持设备已省略).
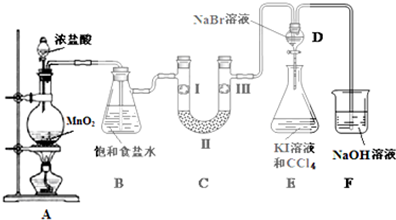
已知:浓硫酸、碱石灰和无水氯化钙均具有吸水性,碱石灰是生石灰和氢氧化钠的混合物.请回答下列问题:
(1)装置A中盛装浓盐酸的仪器名称为分液漏斗,往圆底烧瓶中滴加浓盐酸,反应开始后,圆底烧瓶中发生反应的化学方程式为4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此装置C中Ⅰ、Ⅱ、Ⅲ依次放入d.(填字母)
(4)当向装置D中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为橙色,
装置D中发生反应的离子方程式为2Br-+Cl2=Br2+2Cl-.
(5)打开活塞,将装置D中少量溶液加入装置E中,振荡.观察到的现象是装置E中的溶液分为两层,下层(CCl4层)为紫红色.
(6)装置F中NaOH溶液的作用是吸收多余的氯气,防止污染空气.

已知:浓硫酸、碱石灰和无水氯化钙均具有吸水性,碱石灰是生石灰和氢氧化钠的混合物.请回答下列问题:
(1)装置A中盛装浓盐酸的仪器名称为分液漏斗,往圆底烧瓶中滴加浓盐酸,反应开始后,圆底烧瓶中发生反应的化学方程式为4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此装置C中Ⅰ、Ⅱ、Ⅲ依次放入d.(填字母)
| a | b | c | d | |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| II | 碱石灰 | 浓硫酸 | 碱石灰 | 无水氯化钙 |
| III | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
装置D中发生反应的离子方程式为2Br-+Cl2=Br2+2Cl-.
(5)打开活塞,将装置D中少量溶液加入装置E中,振荡.观察到的现象是装置E中的溶液分为两层,下层(CCl4层)为紫红色.
(6)装置F中NaOH溶液的作用是吸收多余的氯气,防止污染空气.
16.下列有关NaHCO3和Na2CO3的性质比较中,不正确的是( )
0 171248 171256 171262 171266 171272 171274 171278 171284 171286 171292 171298 171302 171304 171308 171314 171316 171322 171326 171328 171332 171334 171338 171340 171342 171343 171344 171346 171347 171348 171350 171352 171356 171358 171362 171364 171368 171374 171376 171382 171386 171388 171392 171398 171404 171406 171412 171416 171418 171424 171428 171434 171442 203614
| A. | 热稳定性:Na2CO3>NaHCO3 | |
| B. | 常温时,在水中的溶解度:Na2CO3>NaHCO3 | |
| C. | 等物质的量的NaHCO3和Na2CO3与足量稀盐酸反应产生CO2的质量:Na2CO3<NaHCO3 | |
| D. | NaHCO3和Na2CO3溶液的物质的量浓度相同时,溶液的pH:Na2CO3>NaHCO3 |
