题目内容
1.实验室配制500mL 0.100mol•L-1的Na2CO3溶液,请回答下列问题:(1)应用托盘天平称取碳酸钠晶体(Na2CO3•10H2O)14.3g.
(2)配制时除应选用托盘天平、药匙、烧杯、玻璃棒外,还需要用到的仪器有500 mL容量瓶、胶头滴管.
(3)容量瓶上标有:①温度、②浓度、③规格、④压强、⑤刻度线这五项中的①③⑤.(填数字符号)
(4)若实验时遇到下列情况,将导致所得溶液浓度偏高的是D.
A.忘记将洗涤液转入容量瓶
B.容量瓶洗涤后内壁有水珠而未作干燥处理
C.定容、摇匀、静置后发现凹液面低于刻度线又加水至刻度线
D.定容时俯视容量瓶的刻度线.
分析 (1)依据m=cVM计算需要溶质的质量;
(2)根据配制一定物质的量浓度溶液步骤选择用到仪器;
(3)依据容量瓶的构造解答;
(4)分析不当操作对溶质的物质的量和溶液的体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)配制500mL 0.100mol•L-1的Na2CO3溶液,需要碳酸钠晶体的质量=0.100mol•L-1×0.5L×286g/mol=14.3g;
故答案为:14.3;
(2)配制一定物质的量浓度溶液步骤:计算、称量、溶解、移液、洗涤、定容、摇匀等,用到的仪器:托盘天平、药匙、烧杯、玻璃棒、500 mL容量瓶、胶头滴管;
还需要的仪器:500 mL容量瓶、胶头滴管;
故答案为:500 mL容量瓶、胶头滴管;
(3)容量瓶上标有:温度、容积、刻度线;
故选:①③⑤;
(4)A.忘记将洗涤液转入容量瓶,导致溶质的物质的量偏小,溶液的浓度偏低,故A不选;
B.容量瓶洗涤后内壁有水珠而未作干燥处理,对溶质的物质的量和溶液的体积都不会产生影响,溶液浓度不变,故B不选;
C.定容、摇匀、静置后发现凹液面低于刻度线又加水至刻度线,导致溶液的体积偏大,溶液的浓度偏小,故C不选;
D.定容时俯视容量瓶的刻度线,导致溶液的体积偏小,溶液的浓度偏大,故D选;
故选:D.
点评 本题考查了配制一定物质的量浓度溶液,明确配制原理和过程是解题关键,题目难度不大,注意容量瓶的构造及使用方法,注意误差分析的方法.

练习册系列答案
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
9.下列物质露置于空气中不易变质的是( )
| A. | 氯水 | B. | 烧碱 | C. | 纯碱 | D. | 漂白粉 |
16.下列有关NaHCO3和Na2CO3的性质比较中,不正确的是( )
| A. | 热稳定性:Na2CO3>NaHCO3 | |
| B. | 常温时,在水中的溶解度:Na2CO3>NaHCO3 | |
| C. | 等物质的量的NaHCO3和Na2CO3与足量稀盐酸反应产生CO2的质量:Na2CO3<NaHCO3 | |
| D. | NaHCO3和Na2CO3溶液的物质的量浓度相同时,溶液的pH:Na2CO3>NaHCO3 |
13.下列各物质的名称不正确的是( )
| A. | 3-甲基-2-戊炔 | B. | 3-甲基-2-丁醇 | C. | 3-甲基-1-丁炔 | D. | 2,2-二甲基丁烷 |
14.将等物质的量的镁和铝混合,取等质量该混合物四份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是( )
| A. | 3 mol•L-1HCl | B. | 4 mol•L-1HNO3 | ||
| C. | 8 mol•L-1NaOH | D. | 18 mol•L-1浓H2SO4 |
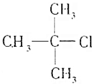 、④
、④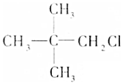 、⑤
、⑤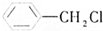 、⑥
、⑥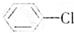 .
.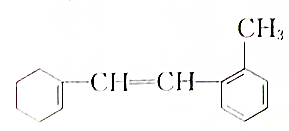 [典型例题√某有机物的结构简式如图:
[典型例题√某有机物的结构简式如图: