19.下列微粒的半径比值大于1的是( )
| A. | Mg2+/Mg | B. | K+/S2- | C. | N/P | D. | Cl-/Cl |
18.已知三种元素,其原子最外层电子数之和为17,核内质子数之和为31,满足上述条件的一组元素是( )
| A. | N P Cl | B. | P O S | C. | N O S | D. | O P Cl |
17.元素性质呈现周期性变化的原因是( )
| A. | 元素原子的原子半径出现周期性变化 | |
| B. | 元素的化合价出现周期性变化 | |
| C. | 元素原子的电子层数出现周期性变化 | |
| D. | 元素原子的核外电子排布出现周期性变化 |
16.属于铝热反应的是( )
| A. | Al+HCl | B. | Al+Fe2O3 | C. | Al+NaOH | D. | Al+O2 |
15.人类未来最理想的燃料是( )
0 171049 171057 171063 171067 171073 171075 171079 171085 171087 171093 171099 171103 171105 171109 171115 171117 171123 171127 171129 171133 171135 171139 171141 171143 171144 171145 171147 171148 171149 171151 171153 171157 171159 171163 171165 171169 171175 171177 171183 171187 171189 171193 171199 171205 171207 171213 171217 171219 171225 171229 171235 171243 203614
| A. | 煤 | B. | 石油 | C. | 氢气 | D. | 天然气 |
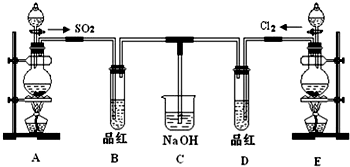
 某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示: 己知A,B、C、D,E五种元素的原子序数依次增大,A元素位于周期表的s区.其原子中电子层数等于未成对电子数:B的基态原子中电子占据三种能量不同的原子轨道,且每种原子轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3 倍. A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,AB两种元素成的原子个数之比为1:1的化合物N是常见的有机溶剂.E有“生物金属”之称,E4+和氩原子的核外电子抹布相同.
己知A,B、C、D,E五种元素的原子序数依次增大,A元素位于周期表的s区.其原子中电子层数等于未成对电子数:B的基态原子中电子占据三种能量不同的原子轨道,且每种原子轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3 倍. A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,AB两种元素成的原子个数之比为1:1的化合物N是常见的有机溶剂.E有“生物金属”之称,E4+和氩原子的核外电子抹布相同.