题目内容
16.属于铝热反应的是( )| A. | Al+HCl | B. | Al+Fe2O3 | C. | Al+NaOH | D. | Al+O2 |
分析 铝热反应是指在高温条件下,铝粉把某些金属氧化物中的金属置换出来的反应;化合物中对应的金属的活泼性比铝弱,该反应将会放出大量的热,其中铝粉和金属氧化物作为铝热剂,镁条和氯酸钾作为引燃剂.
解答 解:A.2Al+6HCl=AlCl3+3H2,该反应不需要高温,且不是金属之间的置换反应,所以不属于铝热反应,故A错误;
B.2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,该反应属于铝热反应,故B正确;
C.2Al+2H2O+2NaOH=2NaAlO2+3H2↑,该反应不需要高温,且不是金属之间的置换反应,所以不属于铝热反应,故C错误;
D.铝和氧气反应生成氧化铝,该反应不是金属之间的置换反应,不属于铝热反应,故D错误;
故选B.
点评 本题考查铝热反应判断,明确铝热反应概念内涵是解本题关键,熟悉铝热反应特点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.少量的金属钠长期暴露在空气中,其最终产物不可能是( )
| A. | Na2CO3 | B. | Na2CO3•7H20 | C. | Na2O2 | D. | Na2CO3•10H20 |
4.(1)海水是巨大的资源宝库,工业上从海水中提取食盐和溴的过程如下:
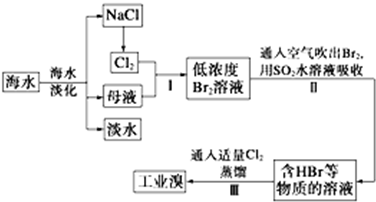
操作Ⅱ发生反应的离子方程式为SO2+Br2+2H2O═SO42-+2Br-+4H+;可以用碳酸钠溶液代替操作Ⅱ中的二氧化硫水溶液,生成物中溴的化合价分别为+5和-1价,操作Ⅲ中如果用稀硫酸代替氯气,则操作Ⅲ中发生反应的离子方程式为BrO3-+5Br-+6H+=3Br2+3H2O.
(2)溴苯是一种化工原料,可以用溴和苯反应合成.实验室合成溴苯的装置示意图如下:
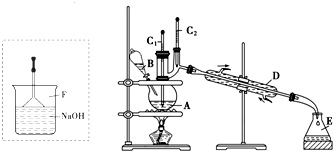
下表为苯、溴和溴苯的相关数据:
回答下列问题:
在A中加入30.0mL无水苯和少量铁屑.在B中小心加入8.0mL液态溴.向A中滴加液溴,反应一段时间后,点燃酒精灯加热蒸馏.
①A的容积最适合的是c(填编号). a.25mL b.50mL c.100mL d.250mL
②收集溴苯时,应根据C2(填“C1”或“C2”)所显示的温度,其温度应为156℃.
③在反应开始后到收集溴苯之前,应先将F装置连接在D装置后,用它可承接的物质有Br2、HBr、C6H6(填化学式).
④某化学小组设计如下实验方案,证明苯和溴发生的是取代反应而不是加成反应.
第一步:取少量反应后F装置中的溶液于试管中;第二步:向其中加入过量的稀硝酸;第三步:继续滴加少量的硝酸银溶液.如果有浅黄色沉淀生成则证明苯和溴发生的是取代反应.该实验方案不合理(填“合理”或“不合理”),理由是溴可以和NaOH溶液反应生成溴离子,也能产生浅黄色沉淀,无法确定是否生成溴化氢,即无法确定两者发生的是取代反应..

操作Ⅱ发生反应的离子方程式为SO2+Br2+2H2O═SO42-+2Br-+4H+;可以用碳酸钠溶液代替操作Ⅱ中的二氧化硫水溶液,生成物中溴的化合价分别为+5和-1价,操作Ⅲ中如果用稀硫酸代替氯气,则操作Ⅲ中发生反应的离子方程式为BrO3-+5Br-+6H+=3Br2+3H2O.
(2)溴苯是一种化工原料,可以用溴和苯反应合成.实验室合成溴苯的装置示意图如下:

下表为苯、溴和溴苯的相关数据:
| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
在A中加入30.0mL无水苯和少量铁屑.在B中小心加入8.0mL液态溴.向A中滴加液溴,反应一段时间后,点燃酒精灯加热蒸馏.
①A的容积最适合的是c(填编号). a.25mL b.50mL c.100mL d.250mL
②收集溴苯时,应根据C2(填“C1”或“C2”)所显示的温度,其温度应为156℃.
③在反应开始后到收集溴苯之前,应先将F装置连接在D装置后,用它可承接的物质有Br2、HBr、C6H6(填化学式).
④某化学小组设计如下实验方案,证明苯和溴发生的是取代反应而不是加成反应.
第一步:取少量反应后F装置中的溶液于试管中;第二步:向其中加入过量的稀硝酸;第三步:继续滴加少量的硝酸银溶液.如果有浅黄色沉淀生成则证明苯和溴发生的是取代反应.该实验方案不合理(填“合理”或“不合理”),理由是溴可以和NaOH溶液反应生成溴离子,也能产生浅黄色沉淀,无法确定是否生成溴化氢,即无法确定两者发生的是取代反应..
11. 25℃时,用Na2S沉淀Cu2+、Zn2+两种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示,下列说法不正确的是( )
25℃时,用Na2S沉淀Cu2+、Zn2+两种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示,下列说法不正确的是( )
 25℃时,用Na2S沉淀Cu2+、Zn2+两种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示,下列说法不正确的是( )
25℃时,用Na2S沉淀Cu2+、Zn2+两种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示,下列说法不正确的是( )| A. | Na2S溶液中:c(S2-)+c(HS-)+c(H2S)═2c(Na+) | |
| B. | 25℃时K甲(CuS)约为1×10-35 | |
| C. | 向100mLZn2+、Cu2+浓度均为10-5mol•L-1的混合溶液中逐滴加入10-4mol•L-1的Na2S溶液,Cu2+先沉淀 | |
| D. | 向Cu2+浓度为10-5mol•L-1的工业废水中加入ZnS粉末,会有CuS沉淀析出 |
8.能制得括号中纯净物的是( )
| A. | 等物质的量的乙烯与氯气加成(1,2-二氯乙烷) | |
| B. | 氯气与乙烷在光照下反应(氯乙烷) | |
| C. | 苯与硝酸在浓硫酸、加热条件下反应(硝基苯) | |
| D. | 乙醇、乙酸与浓H2SO4混合加热(乙酸乙酯) |
6.2011年6月26日是第十七个“国际禁毒日”,其主题是“青少年与合成毒品”.你认为下列各组物质中,都属于毒品的是( )
| A. | 冰毒、阿莫西林 | B. | 海洛因、雷尼替丁 | ||
| C. | 黄曲霉素、诺氟沙星 | D. | 海洛因、摇头丸 |
 醋酸亚铬水合物([Cr(CH3COO)2)]2•2H2O,深红色晶体)是一种氧气吸收剂,通常以二聚体分子存在,不溶于冷水和醚,微溶于醇,易溶于盐酸.实验室制备醋酸亚铬水合物的装置如图所示,涉及的化学方程式如下:
醋酸亚铬水合物([Cr(CH3COO)2)]2•2H2O,深红色晶体)是一种氧气吸收剂,通常以二聚体分子存在,不溶于冷水和醚,微溶于醇,易溶于盐酸.实验室制备醋酸亚铬水合物的装置如图所示,涉及的化学方程式如下: