10.草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的性质,某化学研究性学习小组查阅了有关资料,有关物质的部分性质如下表:
【实验Ⅰ】
探究草酸的不稳定性.用下图中提供的仪器和试剂,验证草酸受热分解得到的混合气体中含有CO和CO2(加热装置和导管等在图中略去,部分装置可以重复使用).
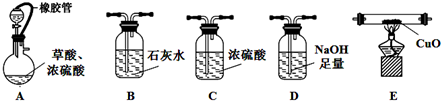
(1)仪器装置正确连接顺序为:ABDCEB.
(2)用上图入提供的装置和试剂实验时,在B中观察到有白色沉淀,也不能说明草酸分解有CO2,请提也改进意见在A与B之间添加一个盛水的洗气瓶,除去草酸蒸气(或在烧瓶上连接冷凝管).
【实验Ⅱ】
实验室用硝酸氧化淀粉水解液法制备草酸.装置如下图所示,反应原理为:
C6H12O6+12HNO3=3H2C2O4+9NO2↑+3NO↑+9H2O
实验步骤如下:
①一定量的淀粉水解液加入三颈烧瓶中
②控制反应温度55-60℃,边搅拌边缓慢滴加一定量的混合酸(65%的HNO3与98%的H2SO4的质量比2:1.25)
③反应3小时,蒸发浓缩、冷却结晶,抽滤后再重结晶得到草酸晶体
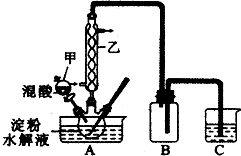
(3)上图实验装置中仪器乙的名称为:冷凝管、装置B的作用安全瓶,防止倒吸、C中试剂是NaOH溶液.
(4)检验淀粉是否水解完全的操作及现像是:取适量水解液于试管中,加入碘水,若溶液变蓝则淀粉水解完全,若溶液不变蓝则淀粉水解不完全.
【实验Ⅲ】
制备草酸亚铁晶体(FeC2O4•2H2O).反应原理为:
FeSO4•(NH4)2SO4•6H2O+H2C2O4=FeC2O4•2H2O+(NH4)2SO4+H2SO4+4H2O
实验步骤如下:
①称取13.7g FeSO4•(NH4)2SO4•6H2O放在200mL烧杯中,然后加30mL蒸馏水和2mL 2mol•L-1 H2SO4,加热溶解.
②再加入40mL 1mol•L-1草酸溶液,加热至沸,然后迅速搅拌(防止暴沸),待有黄色晶体析出后,停止加热,静置.
③弃去上层清液,用40mL蒸馏水充分洗涤晶体,过滤后,再用丙酮洗涤晶体并晾干得4.6g FeC2O4•2H2O
(5)生成的FeC2O4•2H2O需要充分洗涤,检验是否洗涤干净的操作及现像是用小试管取少量最后一次洗涤液,加入BaCl2溶液,如出现白色沉淀,说明沉淀没有洗涤干净,否则,沉淀已洗涤干净.
(6)用丙酮洗涤晶体的目的是减少草酸亚铁晶体的溶解,更快除去草酸亚铁晶体表面的水分.
(7)本实验FeC2O4•2H2O的产率为73.1%.
| 物质 | 物理性质 | 化学性质 |
| 草酸(H2C2O4) | ①易溶于水 ②熔点189.5℃、100℃开始升华 ③草酸钙和草酸氢钙均是白色不溶物 | ①二元弱酸、酸性比碳酸强 ②有毒、具有腐蚀性 ③157℃左右分解、与浓硫酸混合会产生H2O、CO和CO2 |
| 草酸亚铁晶体(FeC2O4•2H2O) | ①浅黄色粉末状晶体 ②微溶于水,难溶于丙酮 | 受热易分解为氧化亚铁或铁单质 |
| 丙酮 | 与水互溶、易挥发 | ---- |
探究草酸的不稳定性.用下图中提供的仪器和试剂,验证草酸受热分解得到的混合气体中含有CO和CO2(加热装置和导管等在图中略去,部分装置可以重复使用).

(1)仪器装置正确连接顺序为:ABDCEB.
(2)用上图入提供的装置和试剂实验时,在B中观察到有白色沉淀,也不能说明草酸分解有CO2,请提也改进意见在A与B之间添加一个盛水的洗气瓶,除去草酸蒸气(或在烧瓶上连接冷凝管).
【实验Ⅱ】
实验室用硝酸氧化淀粉水解液法制备草酸.装置如下图所示,反应原理为:
C6H12O6+12HNO3=3H2C2O4+9NO2↑+3NO↑+9H2O
实验步骤如下:
①一定量的淀粉水解液加入三颈烧瓶中
②控制反应温度55-60℃,边搅拌边缓慢滴加一定量的混合酸(65%的HNO3与98%的H2SO4的质量比2:1.25)
③反应3小时,蒸发浓缩、冷却结晶,抽滤后再重结晶得到草酸晶体

(3)上图实验装置中仪器乙的名称为:冷凝管、装置B的作用安全瓶,防止倒吸、C中试剂是NaOH溶液.
(4)检验淀粉是否水解完全的操作及现像是:取适量水解液于试管中,加入碘水,若溶液变蓝则淀粉水解完全,若溶液不变蓝则淀粉水解不完全.
【实验Ⅲ】
制备草酸亚铁晶体(FeC2O4•2H2O).反应原理为:
FeSO4•(NH4)2SO4•6H2O+H2C2O4=FeC2O4•2H2O+(NH4)2SO4+H2SO4+4H2O
实验步骤如下:
①称取13.7g FeSO4•(NH4)2SO4•6H2O放在200mL烧杯中,然后加30mL蒸馏水和2mL 2mol•L-1 H2SO4,加热溶解.
②再加入40mL 1mol•L-1草酸溶液,加热至沸,然后迅速搅拌(防止暴沸),待有黄色晶体析出后,停止加热,静置.
③弃去上层清液,用40mL蒸馏水充分洗涤晶体,过滤后,再用丙酮洗涤晶体并晾干得4.6g FeC2O4•2H2O
(5)生成的FeC2O4•2H2O需要充分洗涤,检验是否洗涤干净的操作及现像是用小试管取少量最后一次洗涤液,加入BaCl2溶液,如出现白色沉淀,说明沉淀没有洗涤干净,否则,沉淀已洗涤干净.
(6)用丙酮洗涤晶体的目的是减少草酸亚铁晶体的溶解,更快除去草酸亚铁晶体表面的水分.
(7)本实验FeC2O4•2H2O的产率为73.1%.
9.A在一定温度下有分解反应A(s)═B(s)+C(g)+4D(g).若测得生成的气体的质量是同温同压下,相同体积氢气的10倍,且当所生成的气体在标况下的体积为22.4L时,所得B的质量为30.4g,A的摩尔质量为
( )
( )
| A. | 120.4g/mol | B. | 50.4g/mol | C. | 182.4g/mol | D. | 252g/mol |
7.如图是制备和研究乙炔性质的实验装置图.下列说法不正确的是( )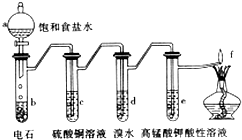

| A. | 制备乙炔的反应原理是CaC2+2H2O→Ca(OH)2+C2H2↑ | |
| B. | c的作用是除去影响后续实验的杂质 | |
| C. | d中的有机产物与AgNO3溶液混合能产生沉淀 | |
| D. | e中的现象说明乙炔不能被高锰酸钾酸性溶液氧化 |
6.某化学实验兴趣小组在“探究氯水与溴化亚铁溶液反应”的实验中发现:“在足量的溴化亚铁溶液中,加入1~2滴氯水,振荡后溶液呈黄色.”
根据已有化学知识及资料,请你参与上述现象形成原因的分析与探究:
(1)提出问题猜想:
猜想Ⅰ:溶液呈黄色是因发生离子反应①2Fe2++Cl2=2Fe3++2Cl-( 填离子方程式)所致.
猜想Ⅱ:溶液呈黄色是因发生离子反应②2Br-+Cl2=Br2+2Cl-( 填离子方程式)所致.
(2)设计实验并验证:
为验证①与②中是哪个原因导致了溶液变黄色,设计并进行了以下实验.请根据以下所给试剂,进行合理选用,完成实验方案1和方案2:
所给试剂:酚酞试液、CCl4、无水酒精、KSCN溶液
方案1:取所述黄色溶液于试管中,滴加KSCN并振荡,溶液变红色;则溶液变黄色由反应①所致.
方案2:取所述黄色溶液于试管中,滴加CCl4并振荡;实验现象为CCl4层(下层)无色.
(3)实验结论:
以上实验不仅验证了溶液变黄的真实原因,同时证明了Fe2+的还原性比Br-
强(填“强”或“弱”).
(4)实验反思:
Ⅰ.根据上述实验推测,若在溴化亚铁溶液中滴入足量氯水,再加入CCl4并充分振荡后静止,产生的现象是溶液分层,上下层均为黄色.
Ⅱ.在100mLFeBr2溶液中通入2.24LCl2(标准状况下),溶液中有1/2的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为1mol/L.
| 『资料』 | 溴水是溴单质的水溶液,因溶有溴单质而呈黄色. |
(1)提出问题猜想:
猜想Ⅰ:溶液呈黄色是因发生离子反应①2Fe2++Cl2=2Fe3++2Cl-( 填离子方程式)所致.
猜想Ⅱ:溶液呈黄色是因发生离子反应②2Br-+Cl2=Br2+2Cl-( 填离子方程式)所致.
(2)设计实验并验证:
为验证①与②中是哪个原因导致了溶液变黄色,设计并进行了以下实验.请根据以下所给试剂,进行合理选用,完成实验方案1和方案2:
所给试剂:酚酞试液、CCl4、无水酒精、KSCN溶液
方案1:取所述黄色溶液于试管中,滴加KSCN并振荡,溶液变红色;则溶液变黄色由反应①所致.
方案2:取所述黄色溶液于试管中,滴加CCl4并振荡;实验现象为CCl4层(下层)无色.
(3)实验结论:
以上实验不仅验证了溶液变黄的真实原因,同时证明了Fe2+的还原性比Br-
强(填“强”或“弱”).
(4)实验反思:
Ⅰ.根据上述实验推测,若在溴化亚铁溶液中滴入足量氯水,再加入CCl4并充分振荡后静止,产生的现象是溶液分层,上下层均为黄色.
Ⅱ.在100mLFeBr2溶液中通入2.24LCl2(标准状况下),溶液中有1/2的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为1mol/L.
4.下表为元素周期表的一部分,参照元素①~⑧在表中的位置,用化学用语回答下列问题
(1)④、⑤、⑥的原子半径由大到小的顺序是Na>Al>O.
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是HNO3>H2CO3>H2SiO3.
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: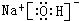 或
或 等.
等.
(4)由表中两种元素的原子按1:1组成的常见液态化合物A的稀溶液易被催化分解,可使用的催化剂为(填序号)
ab.a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)向含有酚酞的NaOH稀溶液中,逐滴滴入10%的上述A溶液,红色很快褪去.褪色原因,甲同学认为A溶液显酸性所致;乙同学认为A溶液强氧化性所致.请你设计一个简单的实验来说明甲对还是乙对.
(简易文字说明)在褪色后的溶液中再逐滴滴入NaOH溶液,若红色不恢复则说明乙对.
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | II A | IIIA | IVA | VA | VIA | VⅡA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是HNO3>H2CO3>H2SiO3.
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
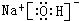 或
或 等.
等.(4)由表中两种元素的原子按1:1组成的常见液态化合物A的稀溶液易被催化分解,可使用的催化剂为(填序号)
ab.a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)向含有酚酞的NaOH稀溶液中,逐滴滴入10%的上述A溶液,红色很快褪去.褪色原因,甲同学认为A溶液显酸性所致;乙同学认为A溶液强氧化性所致.请你设计一个简单的实验来说明甲对还是乙对.
(简易文字说明)在褪色后的溶液中再逐滴滴入NaOH溶液,若红色不恢复则说明乙对.
3.下列离子方程式正确的是( )
| A. | 盐酸中滴加氨水:H++OH-═H2O | |
| B. | 用FeCl3溶液腐蚀铜线路板:Cu+Fe3+═Cu2++Fe2+ | |
| C. | 铜溶于稀硝酸:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| D. | 将氯气溶于水制备次氯酸:Cl2+H2O═2H++Cl-+ClO- |
2.下列实验误差分析错误的是( )
0 171019 171027 171033 171037 171043 171045 171049 171055 171057 171063 171069 171073 171075 171079 171085 171087 171093 171097 171099 171103 171105 171109 171111 171113 171114 171115 171117 171118 171119 171121 171123 171127 171129 171133 171135 171139 171145 171147 171153 171157 171159 171163 171169 171175 171177 171183 171187 171189 171195 171199 171205 171213 203614
| A. | 用湿润的pH试纸测稀碱溶液的pH,测定值偏小 | |
| B. | 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 | |
| C. | 容量瓶中含有少量蒸馏水对所配的溶液无影响 | |
| D. | 测定中和反应的中和热时,保温效果越好,测定误差越小 |
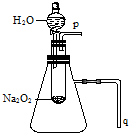 实验:用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
实验:用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.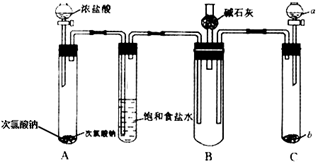
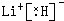 .
.