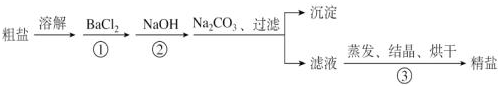
题目内容
9.A在一定温度下有分解反应A(s)═B(s)+C(g)+4D(g).若测得生成的气体的质量是同温同压下,相同体积氢气的10倍,且当所生成的气体在标况下的体积为22.4L时,所得B的质量为30.4g,A的摩尔质量为( )
| A. | 120.4g/mol | B. | 50.4g/mol | C. | 182.4g/mol | D. | 252g/mol |
分析 同温同压下气体的体积比等于物质的量之比,设A的物质的量为1mol,根据方程式可知生成的混合气体的物质的量为5mol,而5molH2的质量是10g,它的10倍是100g,和混合气体与固体B之间的关系,根据质量守恒来求解.
解答 解:同温同压下气体的体积比等于物质的量之比,设A的物质的量为1mol,根据方程式A(s)$\frac{\underline{\;\;△\;\;}}{\;}$B(s)+C(g)+4D(g),可知生成的混合气体的物质的量为5mol,而5molH2的质量是5mol×2g/mol=10g,它的10倍是100g,由方程式可知:
1molB~5mol的混合气体~1molA
5×22.4 1
22.4 n(A)
则:$\frac{5×22.4}{22.4}$所以:n(A)=0.2mol
又因为1molA得到混合气体100g,则0.2molA得到混合气体20g,由质量守恒可知:0.2molA的质量为20g+30.4g=50.4g,
所以M(A)=$\frac{50.4g}{0.2mol}$=252g•mol-1,
故选D.
点评 本题考查有关摩尔质量的相关计算,学生只要灵活运用质量守恒和关系式法就能迅速解题.

练习册系列答案
相关题目
13.取一块金属钠放在燃烧匙里加热,观察到下列现象:①金属先熔化;②在空气中燃烧,产生黄色火花;③燃烧后得到白色固体;④燃烧时火焰为黄色;⑤燃烧后生成浅黄色固体物质.描述正确的是( )
| A. | ①② | B. | ①②③ | C. | ①④ | D. | ①④⑤ |
20.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 用含0.lmolFeCl3的溶液与足量沸水反应制得的Fe(0H)3胶体中胶粒数为0.1NA | |
| B. | 46g N02和N204的混合气体中含原子总数为NA | |
| C. | 标准状况下,5.6L CCl4含有的分子数为0.25NA | |
| D. | 0.25 mol Na2O2中含有的阴离子数为0.5 NA |
17.甲酯丙烯酸甲酯(CH2=C(CH3)COOCH3)是合成有机玻璃的单体.
旧法合成的反应是:①(CH3)2C=O+HCN→(CH3)2(OH)CN
②(CH3)2C(OH)CN+CH3OH+H2SO4→CH2=C(CH3)COOCH3+NH4HSO4
新法合成的反应是:CH3C≡CH+CO+CH3OH$\stackrel{Pb}{→}$CH2=C(CH3)COOCH3,与旧法相比,新法的突出优点是( )
旧法合成的反应是:①(CH3)2C=O+HCN→(CH3)2(OH)CN
②(CH3)2C(OH)CN+CH3OH+H2SO4→CH2=C(CH3)COOCH3+NH4HSO4
新法合成的反应是:CH3C≡CH+CO+CH3OH$\stackrel{Pb}{→}$CH2=C(CH3)COOCH3,与旧法相比,新法的突出优点是( )
| A. | 原料无爆炸危险 | B. | 原料都是无毒物质 | ||
| C. | 没有副产物,原料利用率高 | D. | 对设备腐蚀性较小 |
4.下表为元素周期表的一部分,参照元素①~⑧在表中的位置,用化学用语回答下列问题
(1)④、⑤、⑥的原子半径由大到小的顺序是Na>Al>O.
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是HNO3>H2CO3>H2SiO3.
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: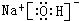 或
或 等.
等.
(4)由表中两种元素的原子按1:1组成的常见液态化合物A的稀溶液易被催化分解,可使用的催化剂为(填序号)
ab.a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)向含有酚酞的NaOH稀溶液中,逐滴滴入10%的上述A溶液,红色很快褪去.褪色原因,甲同学认为A溶液显酸性所致;乙同学认为A溶液强氧化性所致.请你设计一个简单的实验来说明甲对还是乙对.
(简易文字说明)在褪色后的溶液中再逐滴滴入NaOH溶液,若红色不恢复则说明乙对.
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | II A | IIIA | IVA | VA | VIA | VⅡA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是HNO3>H2CO3>H2SiO3.
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
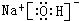 或
或 等.
等.(4)由表中两种元素的原子按1:1组成的常见液态化合物A的稀溶液易被催化分解,可使用的催化剂为(填序号)
ab.a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)向含有酚酞的NaOH稀溶液中,逐滴滴入10%的上述A溶液,红色很快褪去.褪色原因,甲同学认为A溶液显酸性所致;乙同学认为A溶液强氧化性所致.请你设计一个简单的实验来说明甲对还是乙对.
(简易文字说明)在褪色后的溶液中再逐滴滴入NaOH溶液,若红色不恢复则说明乙对.
1.下列各组物质中化学键的类型相同的是( )
| A. | HCl MgCl2 NH4Cl | B. | H2O Na2O ? CO2 | ||
| C. | CaCl2 ? NaOH H2O | D. | NH3 H2O CO2 |
18.两种气态烃的混合物共0.1mol,充分燃烧后得3.58L(标准状况下)CO2和3.6g水,下列说法正确的是( )
| A. | 一定有甲烷 | B. | 一定有乙烯 | C. | 可能有乙烷 | D. | 无法计算 |