5.Q、M、N三种含碳物质互为同系物,下列有关说法中不正确的是( )
| A. | 若Q、M为烯烃,则N可以使溴的CCl4溶液褪色 | |
| B. | 若Q、M均为一元羧酸,则N的分子式可能是CH2O2 | |
| C. | 三种物质的组成元素相同,相对分子质量相同 | |
| D. | 三种物质的分子结构相似,分子组成相差若干个“CH2”基团 |
4.下列各组反应与乙酸官能团中O-H键的断裂无关的是( )
| A. | 乙酸+Na2CO3 | B. | 乙酸+NaOH | C. | 乙酸+乙醇 | D. | 乙酸+Fe |
3.CH3CH=CHCOOH,该有机物能发生的反应是( )
①取代反应 ②加成反应 ③使溴水褪色④使酸性KMnO4溶液褪色 ⑤酯化反应 ⑥聚合反应.
①取代反应 ②加成反应 ③使溴水褪色④使酸性KMnO4溶液褪色 ⑤酯化反应 ⑥聚合反应.
| A. | 以上反应均可发生 | B. | 只有⑤不能发生 | ||
| C. | 只有⑥不能发生 | D. | 只有②不能发生 |
2.下列化学用语书写正确的是( )
| A. | 氯离子的结构示意图: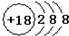 | |
| B. | HClO的结构式为:H-Cl-O | |
| C. | 氯化镁的电子式: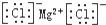 | |
| D. | 用电子式表示氯化氢分子的形成过程: |
1.升高温度,下列常数中不一定增大的是( )
| A. | 平衡常数K | B. | 电离常数Ka | ||
| C. | 水的离子积常数Kw | D. | 盐的水解常数Kh |
20.化学与生产、生活、社会密切相关.下列有关说法中,错误的是( )
| A. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| B. | 血液透析是利用了胶体的性质 | |
| C. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| D. | 点燃爆竹后,硫燃烧生成SO3 |
19.1.52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况),向反应后的溶液中加入1.0mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是( )
| A. | 得到2.54 g沉淀时,加入NaOH溶液的体积是700 mL | |
| B. | 该合金中铜与镁的物质的量之比是2:1 | |
| C. | 该浓硝酸中HNO3的物质的量浓度是14.0 mol/L | |
| D. | NO2和N2O4的混合气体中,NO2的体积分数是80% |
18.下列指定反应的离子方程式正确的是( )
| A. | Fe和足量稀硝酸反应Fe+2H+═Fe2++H2↑ | |
| B. | 将Fe(NO3)3溶液与少量HI混合:8H++2NO3-+6I-═4H2O+3I2+2NO↑ | |
| C. | 用过量氨水吸收SO2的反应:NH3•H2O+SO2═NH4++HSO3- | |
| D. | 少量Ca(OH)2和NaHCO3反应 Ca2++OH-+HCO3-═CaCO3↓+H2O |
17.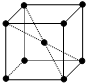 金属钠晶体为体心立方晶体(晶胞如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(mol-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )
金属钠晶体为体心立方晶体(晶胞如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(mol-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )
 金属钠晶体为体心立方晶体(晶胞如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(mol-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )
金属钠晶体为体心立方晶体(晶胞如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(mol-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )| A. | 3$\sqrt{\frac{2a}{{N}_{Aρ}}}$ | B. | $\sqrt{3}$×3$\sqrt{\frac{2a}{{N}_{Aρ}}}$ | C. | $\frac{\sqrt{3}}{4}$×3$\sqrt{\frac{2a}{{N}_{Aρ}}}$ | D. | $\frac{1}{2}$×3$\sqrt{\frac{2a}{{N}_{Aρ}}}$ |
16.元素的原子核外有四个电子层,其3d能级上的电子数是4s能级上的3倍,则此元素是( )
0 171001 171009 171015 171019 171025 171027 171031 171037 171039 171045 171051 171055 171057 171061 171067 171069 171075 171079 171081 171085 171087 171091 171093 171095 171096 171097 171099 171100 171101 171103 171105 171109 171111 171115 171117 171121 171127 171129 171135 171139 171141 171145 171151 171157 171159 171165 171169 171171 171177 171181 171187 171195 203614
| A. | S | B. | Fe | C. | Si | D. | Cl |