1.某化学小组进行了硫代硫酸钠(Na2S2O3)的探究,首先通过查阅资料得到如下信息:a.Na2S2O3、BaS2O3均易溶于水;b.Na2S2O3晶体在空气中易被氧化.然后进行如下实验: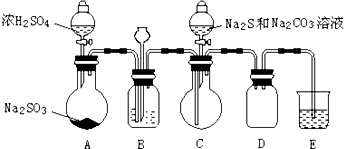
【实验一】硫代硫酸钠(Na2S2O3)的制取实验室制备装置如图所示(夹持装置已省略):
回答问题:
(1)①装置B中的长颈漏斗的作用是平衡压强.
②B中最好盛装的液体是c.
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(2)在装置C中有Na2S2O3生成.
①写出装置C中反应的化学方程式:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2
②结束反应后,取C中溶液,经蒸发浓缩、冷却结晶、过滤洗涤、干燥,得到Na2S2O3•5H2O.
(3)装置E中为NaOH溶液.
【实验二】硫代硫酸钠(Na2S2O3)的性质
(4)Na2S2O3在酸性溶液中不能稳定存在.请用离子方程式表示该过程:2H++S2O32-=SO2↑+S↓+H2O
(5)如何检验Na2S2O3晶体在空气中已被氧化?少量Na2S2O3晶体于试管中,加适量水溶解,滴加少量的氯化钡溶液,如有白色沉淀生成,说明已被氧化.
【实验三】用Na2S2O3测定废水中的Ba2+
(6)工业上常用Na2S2O3溶液测定废水中Ba2+的浓度,步骤如下:取废水25.00mL,控制适当的酸度加入足量 K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解,此时CrO42-全部转化为Cr2O72-;再加过KI溶液,充分反应后得混合溶液V mL,将其平均分成4等份,加入淀粉溶液作指示剂,用0.001 00mol•L-1 的Na2S2O3溶液进行滴定,反应完全时,相关数据记录如表所示:
部分反应离子方程式为:
Cr2O72-+6I-+14H+═2Cr3++3I2+7H2O;
I2+2S2O32-═2I-+S4O64-.
①判断达到滴定终点的现象是滴加最后一滴Na2S2O3标准液时溶液由蓝色变为无色且半分钟内不变色,
②计算废水中Ba2+的物质的量浓度9.6×10-4mol•L-1.

【实验一】硫代硫酸钠(Na2S2O3)的制取实验室制备装置如图所示(夹持装置已省略):
回答问题:
(1)①装置B中的长颈漏斗的作用是平衡压强.
②B中最好盛装的液体是c.
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(2)在装置C中有Na2S2O3生成.
①写出装置C中反应的化学方程式:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2
②结束反应后,取C中溶液,经蒸发浓缩、冷却结晶、过滤洗涤、干燥,得到Na2S2O3•5H2O.
(3)装置E中为NaOH溶液.
【实验二】硫代硫酸钠(Na2S2O3)的性质
(4)Na2S2O3在酸性溶液中不能稳定存在.请用离子方程式表示该过程:2H++S2O32-=SO2↑+S↓+H2O
(5)如何检验Na2S2O3晶体在空气中已被氧化?少量Na2S2O3晶体于试管中,加适量水溶解,滴加少量的氯化钡溶液,如有白色沉淀生成,说明已被氧化.
【实验三】用Na2S2O3测定废水中的Ba2+
(6)工业上常用Na2S2O3溶液测定废水中Ba2+的浓度,步骤如下:取废水25.00mL,控制适当的酸度加入足量 K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解,此时CrO42-全部转化为Cr2O72-;再加过KI溶液,充分反应后得混合溶液V mL,将其平均分成4等份,加入淀粉溶液作指示剂,用0.001 00mol•L-1 的Na2S2O3溶液进行滴定,反应完全时,相关数据记录如表所示:
| 实验编号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准 溶液的体积/mL | 18.02 | 17.98 | 18.00 | 20.03 |
Cr2O72-+6I-+14H+═2Cr3++3I2+7H2O;
I2+2S2O32-═2I-+S4O64-.
①判断达到滴定终点的现象是滴加最后一滴Na2S2O3标准液时溶液由蓝色变为无色且半分钟内不变色,
②计算废水中Ba2+的物质的量浓度9.6×10-4mol•L-1.
20.有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色粘稠液体,易溶于水.为研究A的组成和结构,进行如下实验:
已知:①2R-COOH+2Na→2R-COONa+H2↑
②R-COOH+NaHCO3→R-COONa+CO2↑+H2O
已知:①2R-COOH+2Na→2R-COONa+H2↑
②R-COOH+NaHCO3→R-COONa+CO2↑+H2O
| 实验步骤 | 解释或实验结论 |
| (1)取9.0g有机物A加热使其气化,测得其密度是相同条件下H2的45倍 | (1)由此可知A的相对分子质量为90. |
| (2)将9.0gA在足量O2中充分燃烧,其产物依次缓缓通过浓硫酸、碱石灰,两者分别增重5.4g和13.2g. | (2)由此可知A的分子式为C3H6O3. |
| (3)另取A9.0g,跟足量的NaHCO3粉末反应,生成CO2气体2.24L;9.0gA若与足量金属钠反应生成H2也是2.24L(气体体积皆为标准状况下测得). | (3)由此可知A中含有官能团有.(填结构简式)-COOH、-OH |
(4)A的核磁共振氢谱如下图: | (4)由此可知A中含有4种不同性质的氢原子 (5)综上,A的结构简式为  . . |
16.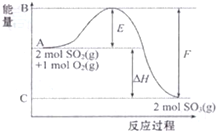 2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1,该反应过程能量变化如图所示,下列叙述中正确的是( )
2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1,该反应过程能量变化如图所示,下列叙述中正确的是( )
0 170683 170691 170697 170701 170707 170709 170713 170719 170721 170727 170733 170737 170739 170743 170749 170751 170757 170761 170763 170767 170769 170773 170775 170777 170778 170779 170781 170782 170783 170785 170787 170791 170793 170797 170799 170803 170809 170811 170817 170821 170823 170827 170833 170839 170841 170847 170851 170853 170859 170863 170869 170877 203614
 2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1,该反应过程能量变化如图所示,下列叙述中正确的是( )
2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1,该反应过程能量变化如图所示,下列叙述中正确的是( )| A. | 该反应的反应物总能量小于生成物总能量 | |
| B. | 该反应的逆反应为吸热反应 | |
| C. | 图中△H=-99kJ•mol-1, | |
| D. | 图中字母E所示能量值表示该反应的活化能 |

 化学能和电能的相互转化是能量转化的重要形式,电池在现代生活的很多方面得到广泛应用.
化学能和电能的相互转化是能量转化的重要形式,电池在现代生活的很多方面得到广泛应用.
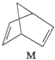 $?_{暗处}^{光照}$
$?_{暗处}^{光照}$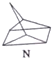 △H=+88.6kJ•mol-1
△H=+88.6kJ•mol-1