题目内容
16.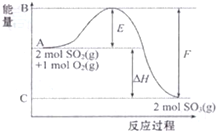 2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1,该反应过程能量变化如图所示,下列叙述中正确的是( )
2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1,该反应过程能量变化如图所示,下列叙述中正确的是( )| A. | 该反应的反应物总能量小于生成物总能量 | |
| B. | 该反应的逆反应为吸热反应 | |
| C. | 图中△H=-99kJ•mol-1, | |
| D. | 图中字母E所示能量值表示该反应的活化能 |
分析 A、C分别表示反应物总能量的生成物总能量,E为活化能,活化能的大小与反应热无关,可逆反应中两个方向的反应热大小相同符符号相反.
解答 解:A.图中A、C分别表示反应物总能量和生成物总能量,并且反应物总能量大于生成物总能量,故A错误;
B.反应物总能量大于生成物总能量,则该反应为放热反应,所以逆反应为吸热反应,故B正确;
C.已2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1,所以图中△H=-198kJ•mol-1,故C错误;
D.图中字母E表示该反应的活化能,故D正确;
故选BD.
点评 本题考查反应过程的能量变化图以及热化学方程式,题目难度不大,注意活化能与反应热的关系.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
4.下列说法正确的是( )
| A. | 淀粉水解产物是CO2和H2O | B. | 油脂水解产物有氨基酸 | ||
| C. | 蔗糖与果糖互为同分异构体 | D. | 蛋白质是人类重要营养物质 |
11.可以通过图示装置实现下列实验目的是( )

| A. | 分离乙酸和乙酸乙酯 | B. | 分离苯和苯酚钠溶液 | ||
| C. | 分离苯和硝基苯 | D. | 分离苯和溴苯 |
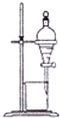
1.某化学小组进行了硫代硫酸钠(Na2S2O3)的探究,首先通过查阅资料得到如下信息:a.Na2S2O3、BaS2O3均易溶于水;b.Na2S2O3晶体在空气中易被氧化.然后进行如下实验:
【实验一】硫代硫酸钠(Na2S2O3)的制取实验室制备装置如图所示(夹持装置已省略):
回答问题:
(1)①装置B中的长颈漏斗的作用是平衡压强.
②B中最好盛装的液体是c.
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(2)在装置C中有Na2S2O3生成.
①写出装置C中反应的化学方程式:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2
②结束反应后,取C中溶液,经蒸发浓缩、冷却结晶、过滤洗涤、干燥,得到Na2S2O3•5H2O.
(3)装置E中为NaOH溶液.
【实验二】硫代硫酸钠(Na2S2O3)的性质
(4)Na2S2O3在酸性溶液中不能稳定存在.请用离子方程式表示该过程:2H++S2O32-=SO2↑+S↓+H2O
(5)如何检验Na2S2O3晶体在空气中已被氧化?少量Na2S2O3晶体于试管中,加适量水溶解,滴加少量的氯化钡溶液,如有白色沉淀生成,说明已被氧化.
【实验三】用Na2S2O3测定废水中的Ba2+
(6)工业上常用Na2S2O3溶液测定废水中Ba2+的浓度,步骤如下:取废水25.00mL,控制适当的酸度加入足量 K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解,此时CrO42-全部转化为Cr2O72-;再加过KI溶液,充分反应后得混合溶液V mL,将其平均分成4等份,加入淀粉溶液作指示剂,用0.001 00mol•L-1 的Na2S2O3溶液进行滴定,反应完全时,相关数据记录如表所示:
部分反应离子方程式为:
Cr2O72-+6I-+14H+═2Cr3++3I2+7H2O;
I2+2S2O32-═2I-+S4O64-.
①判断达到滴定终点的现象是滴加最后一滴Na2S2O3标准液时溶液由蓝色变为无色且半分钟内不变色,
②计算废水中Ba2+的物质的量浓度9.6×10-4mol•L-1.

【实验一】硫代硫酸钠(Na2S2O3)的制取实验室制备装置如图所示(夹持装置已省略):
回答问题:
(1)①装置B中的长颈漏斗的作用是平衡压强.
②B中最好盛装的液体是c.
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(2)在装置C中有Na2S2O3生成.
①写出装置C中反应的化学方程式:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2
②结束反应后,取C中溶液,经蒸发浓缩、冷却结晶、过滤洗涤、干燥,得到Na2S2O3•5H2O.
(3)装置E中为NaOH溶液.
【实验二】硫代硫酸钠(Na2S2O3)的性质
(4)Na2S2O3在酸性溶液中不能稳定存在.请用离子方程式表示该过程:2H++S2O32-=SO2↑+S↓+H2O
(5)如何检验Na2S2O3晶体在空气中已被氧化?少量Na2S2O3晶体于试管中,加适量水溶解,滴加少量的氯化钡溶液,如有白色沉淀生成,说明已被氧化.
【实验三】用Na2S2O3测定废水中的Ba2+
(6)工业上常用Na2S2O3溶液测定废水中Ba2+的浓度,步骤如下:取废水25.00mL,控制适当的酸度加入足量 K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解,此时CrO42-全部转化为Cr2O72-;再加过KI溶液,充分反应后得混合溶液V mL,将其平均分成4等份,加入淀粉溶液作指示剂,用0.001 00mol•L-1 的Na2S2O3溶液进行滴定,反应完全时,相关数据记录如表所示:
| 实验编号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准 溶液的体积/mL | 18.02 | 17.98 | 18.00 | 20.03 |
Cr2O72-+6I-+14H+═2Cr3++3I2+7H2O;
I2+2S2O32-═2I-+S4O64-.
①判断达到滴定终点的现象是滴加最后一滴Na2S2O3标准液时溶液由蓝色变为无色且半分钟内不变色,
②计算废水中Ba2+的物质的量浓度9.6×10-4mol•L-1.
8.E,F,Z,W为短周期元素,原子半径E>F>Z>W,E,F,Z处于同一周期,Z、W处于同一主族,E、F、Z原子序数之和为40,E是短周期中除稀有气体元素外半径最大的元素.下列说法正确的是( )
| A. | 若E、F、W形成的化合物EFW2,则E与W可以形成化合物E2W2 | |
| B. | F的最高价氧化物对应的水化物一定能与氢氧化钠溶液反应 | |
| C. | 稳定性:Z的氢化物>W的氢化物 | |
| D. | 沸点:Z的氢化物>W的氢化物 |
5.化学与科技、社会、生活、生产密切结合,下列有关说法不正确的是( )
| A. | “乙醇汽油”的广泛使用能有效减少有害气体的排放 | |
| B. | 误食重金属盐而引起的中毒,急救方法是服用大量的豆浆或牛奶 | |
| C. | “无氟冰箱”取代“含氟冰箱”,对人类的保护伞一臭氧层起到保护作用 | |
| D. | “海水淡化”可以解决“淡水供应危机”,向海水中加人净水剂明矾可以使海水淡化 |
6.下列化合物中既易发生取代反应,也可发生加成反应,还能使KMnO4酸性溶液褪色的是( )
| A. | 乙烷 | B. | 乙醇 | C. | 甲苯 | D. | 苯 |
 为除去粗盐NaCl中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂均过量):
为除去粗盐NaCl中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂均过量):