9.已知非金属单质A2、B2、C2之间能发生如下反应:A2+2B-=2A-+B2,B2+2C-=2B-+C2.以下说法正确的是( )
| A. | 氧化性:A2>B2>C2 | B. | 还原性:A->B->C- | ||
| C. | 单质活动性:C2>B2>A2 | D. | 反应:A2+2C-=2A-+C2不能发生 |
8.下列离子方程式中不正确的是( )
| A. | 工业上制取Cl2:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$ 2OH-+Cl2↑+H2↑ | |
| B. | 碘化钾溶液跟适量溴水反应:2I-+Br2=I2+2Br- | |
| C. | 将金属钠加入水中:Na+2H2O=Na++2OH-+H2↑ | |
| D. | 将氯气通入氯化亚铁溶液中:2Fe2++Cl2=2Fe3++2Cl- |
7.SO2能使浸过溴水的滤纸褪色,这说明了( )
| A. | SO2具有漂白性 | B. | 溴具有氧化性 | C. | SO2具有氧化性 | D. | 溴具有挥发性 |
6.下列有关物质用途的叙述中,不正确的是( )
| A. | 二氧化硅可以用于制造变压器的铁芯材料 | |
| B. | 硫可用于制造黑火药 | |
| C. | 二氧化硅可用于制造光导纤维 | |
| D. | 氢氧化铝既能吸附水中悬浮物,又能吸附色素,故可用于净水 |
3.某溶液中可能含有:Na+、Mg2+、Fe2+、Fe3+、I-、Cl-、NO3-、CO32-、SO42-中的几种(不考虑水的电离和离子的水解因素),各离子浓度均0.1mol•L-1.往该溶液中加入过量稀盐酸,溶液颜色变深且阴离子种类不变,下列说法不正确的是( )
| A. | 溶液颜色变深可能是Fe2+或I-被氧化 | |
| B. | 原溶液中肯定含有Fe2+、Cl-、NO3-,肯定不含有Na+、Fe3+、I-、CO32- | |
| C. | 取少量原溶液,加入盐酸酸化的BaCl2溶液,若有白色沉淀产生,则原溶液中含有Mg2+ | |
| D. | 该溶液中是否存在Na+,无需通过焰色反应确定 |
2.某锂离子电池的总反应为:Li1-xFePO4+LixC6$?_{充电}^{放电}$C6+LiFePO4,(LixC6表示锂原子嵌入石墨形成的复合材料),其工作原理如图所示.下列说法不正确的是( )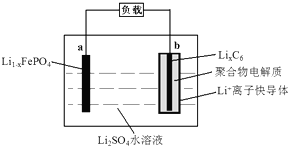

| A. | 放电时,电流从a极经负载后流向b极 | |
| B. | 充电时,Li+向a极移动 | |
| C. | 充电时a极发生的反应为:LiFePO4-xe-=Li1-xFePO4+xLi+ | |
| D. | 放电时,每转移xmol电子,产生1mol C6 |
1.下列说法正确的是( )
0 170668 170676 170682 170686 170692 170694 170698 170704 170706 170712 170718 170722 170724 170728 170734 170736 170742 170746 170748 170752 170754 170758 170760 170762 170763 170764 170766 170767 170768 170770 170772 170776 170778 170782 170784 170788 170794 170796 170802 170806 170808 170812 170818 170824 170826 170832 170836 170838 170844 170848 170854 170862 203614
| A. | 要证明硫酸亚铁铵晶体中含有NH4+,可以取少量晶体溶于水,加入足量NaOH浓溶液并加热,再用湿润的蓝色石蕊试纸检验产生的气体 | |
| B. | KClO3、KNO3、KMnO4等强氧化剂或其混合物不能研磨,否则将引起爆炸 | |
| C. | 常温下用pH试纸分别测定0.1mol•L-1NaClO溶液和0.01mol•L-1NaClO溶液的pH,可以比较浓度对水解程度的影响 | |
| D. | 过滤、结晶、灼烧、萃取、分液和蒸馏等都是常用的分离有机混合物的方法 |
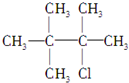
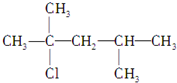
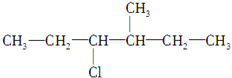
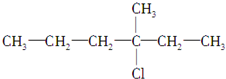
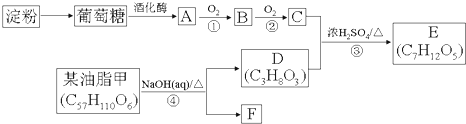
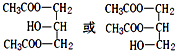 .
.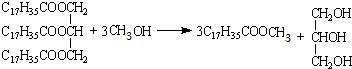 .
.