题目内容
8.下列离子方程式中不正确的是( )| A. | 工业上制取Cl2:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$ 2OH-+Cl2↑+H2↑ | |
| B. | 碘化钾溶液跟适量溴水反应:2I-+Br2=I2+2Br- | |
| C. | 将金属钠加入水中:Na+2H2O=Na++2OH-+H2↑ | |
| D. | 将氯气通入氯化亚铁溶液中:2Fe2++Cl2=2Fe3++2Cl- |
分析 A.电解饱和食盐水制备氯气;
B.发生氧化还原反应,遵循电子、电荷守恒;
C.电子、电荷不守恒;
D.反应生成氯化铁,电子、电荷守恒.
解答 解:A.惰性电极电解饱和食盐水制备氯气的离子反应为2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$ 2OH-+Cl2↑+H2↑,故A正确;
B.碘化钾溶液跟适量溴水反应的离子反应为2I-+Br2=I2+2Br-,故B正确;
C.将金属钠加入水中的离子反应为2Na+2H2O=2Na++2OH-+H2↑,故C错误;
D.将氯气通入氯化亚铁溶液中的离子反应为2Fe2++Cl2=2Fe3++2Cl-,故D正确;
故选C.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒分析,题目难度不大.

练习册系列答案
相关题目
19.下列溶液中,溶质的物质的量浓度为1mol/L的是( )
| A. | 将40 g NaOH溶于1 L水所得的溶液 | |
| B. | 将80 g SO3溶于水并配成1 L的溶液 | |
| C. | 将0.5 mol/L的NaNO3溶液100 mL加热蒸发掉50 g水的溶液 | |
| D. | 含K+为2 mol的K2SO4溶液 |
16.某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、HCO3-等离子.当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,下列说法正确的是( )
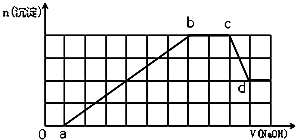

| A. | 原溶液中含有的Fe3+和Al3+的物质的量之比为1:1 | |
| B. | ab段发生的离子反应为:Al3++3OH-=Al(OH)3↓,Mg2++2OH-=Mg(OH)2↓ | |
| C. | 原溶液中含有的阳离子必定有H+、NH4+、Al3+、Mg2+ | |
| D. | d点溶液中含有的溶质只有Na2SO4 |
3.某溶液中可能含有:Na+、Mg2+、Fe2+、Fe3+、I-、Cl-、NO3-、CO32-、SO42-中的几种(不考虑水的电离和离子的水解因素),各离子浓度均0.1mol•L-1.往该溶液中加入过量稀盐酸,溶液颜色变深且阴离子种类不变,下列说法不正确的是( )
| A. | 溶液颜色变深可能是Fe2+或I-被氧化 | |
| B. | 原溶液中肯定含有Fe2+、Cl-、NO3-,肯定不含有Na+、Fe3+、I-、CO32- | |
| C. | 取少量原溶液,加入盐酸酸化的BaCl2溶液,若有白色沉淀产生,则原溶液中含有Mg2+ | |
| D. | 该溶液中是否存在Na+,无需通过焰色反应确定 |
20.下列说法正确的是( )
| A. | 按系统命名法,烷烃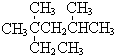 的名称是2,4-二甲基-2-乙基戊烷 的名称是2,4-二甲基-2-乙基戊烷 | |
| B. | 常压下,正戊烷、异戊烷、新戊烷的沸点依次增大 | |
| C. | 糖类、油脂、蛋白质都是高分子化合物,一定条件下都能发生水解反应 | |
| D. | 丙烯酸(CH2═CH-COOH)能发生取代、氧化、还原、加聚反应 |
17.下列物质中,不可以通过乙烯加成反应得到的是( )
| A. | CH3CH3 | B. | CH3CH2Br | C. | CH3CH2OH | D. | CH3CHCl2 |
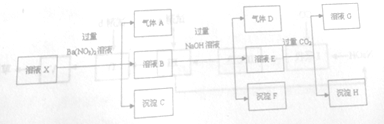
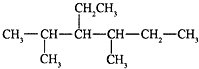 2,4二甲基-3-乙基己烷
2,4二甲基-3-乙基己烷