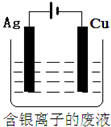
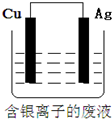
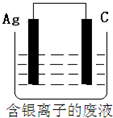
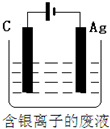
3.下列说法正确的是( )
| A. | 做衣服的棉和麻均与淀粉互为同分异构体 | |
| B. | 向蔗糖水解后所得溶液中加入新制Cu(OH)2煮沸会析出砖红色沉淀 | |
| C. | 煎炸食物的花生油和牛油都是可皂化的饱和酯类 | |
| D. | 误食重金属盐而引起的中毒可服用大量豆浆或牛奶进行解救 |
2.下列各组离子在给定条件的溶液中可能大量共存的是( )
| A. | 加入铝粉有大量氢气产生的溶液中:Mg2+、K+、NO3-、SiO32- | |
| B. | 在0.1mol/L氢氧化钠的溶液中:Na+、K+、Cr2O72-、S2- | |
| C. | 在0.1mol/L的醋酸溶液中:Fe2+、Na+、ClO-、Ca2+ | |
| D. | 在0.1mol/L的硝酸溶液中:NH4+、Ca2+、Cl-、K+ |
20.下列有关元素非金属性的比较,正确的是( )
| A. | 进行H2O和H2S的热分解实验,确定硫和氧两种元素的非金属性强弱 | |
| B. | HCl溶液的酸性比H2S溶液的酸性强,则氯元素的非金属性比硫强 | |
| C. | H2O的沸点高于H2S,则氧元素的非金属性强于硫元素 | |
| D. | 浓H2SO4的氧化性强于HClO4,可确定硫和氯两种元素的非金属性强弱 |
16.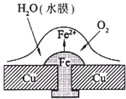 已知铅蓄电池的总反应PbO2+Pb+2H2SO4 $?_{充电}^{放电}$ 2PbSO4+2H2O,图为铁铆钉铆在铜板上,有关叙述不正确的是( )
已知铅蓄电池的总反应PbO2+Pb+2H2SO4 $?_{充电}^{放电}$ 2PbSO4+2H2O,图为铁铆钉铆在铜板上,有关叙述不正确的是( )
 已知铅蓄电池的总反应PbO2+Pb+2H2SO4 $?_{充电}^{放电}$ 2PbSO4+2H2O,图为铁铆钉铆在铜板上,有关叙述不正确的是( )
已知铅蓄电池的总反应PbO2+Pb+2H2SO4 $?_{充电}^{放电}$ 2PbSO4+2H2O,图为铁铆钉铆在铜板上,有关叙述不正确的是( )| A. | 铅蓄电池放电时,电路中每转移2mol电子,生成1mol硫酸铅 | |
| B. | 如图,铁铆钉发生吸氧腐蚀,在铁钉附近滴加K3[Fe(CN)6]溶液,可观察铁钉附近有蓝色沉淀产生 | |
| C. | 铅蓄电池充电时,阳极电极反应为 PbSO4+2H2O-2e-═PbO2+4H++SO42- | |
| D. | 铅蓄电池放电时,内电路硫酸根离子向铅极移动,正极附近溶液的pH增大 |
15.25℃时,下列各溶液中关系的叙述中,正确的是( )
| A. | 0.1 mol/L HA(某酸)溶液pH≠1,0.1 mol/L BOH(某碱)溶液中c(OH-)=0.1 mol/L,则BA(盐)溶液pH<7 | |
| B. | pH=2的盐酸与pH=l的硫酸溶液中c(H+)之比为2:1 | |
| C. | pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则c (Na+)+c(H+)=c(OH-)+c(CH3COO-) | |
| D. | 4种pH相同的溶液①CH3COONa ②NaHCO3 ③NaOH中c(Na+)的大小顺序是②>①>③ |
14.0.1mol Na2SO4溶解在( )mol H2O中,才能使100个H2O中含1个Na+.
0 170626 170634 170640 170644 170650 170652 170656 170662 170664 170670 170676 170680 170682 170686 170692 170694 170700 170704 170706 170710 170712 170716 170718 170720 170721 170722 170724 170725 170726 170728 170730 170734 170736 170740 170742 170746 170752 170754 170760 170764 170766 170770 170776 170782 170784 170790 170794 170796 170802 170806 170812 170820 203614
| A. | 20 mol | B. | 10 mol | C. | 5 mol | D. | 30 mol |