8.下列能导电的物质是( )
| A. | 固态NaOH | B. | 酒精 | C. | 液态氯化氢 | D. | NaCl溶液 |
7.柴静的调查报告《苍穹之下》引起人们对雾霾的更大关注.某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5微米的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样,测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断试样的pH=4.
(2)洗涤含SO2的烟气,下列物质可作洗涤剂的是bc
a.CaCl2 溶液 b.Na2CO3 溶液 c.Ca(OH)2 悬浊液 d.浓H2SO4
(3)安装汽车尾气催化转化器也可减轻PM2.5的危害,其反应是:
2NO(g)+2CO(g)$\frac{\underline{\;催化剂\;}}{\;}$2CO2(g)+N2(g);△H<0
①该反应平衡常数表达式K=$\frac{{c}^{2}(C{O}_{2})c({N}_{2})}{{c}^{2}(NO){c}^{2}(CO)}$;温度升高K值减小(填“增大”或“减小”)
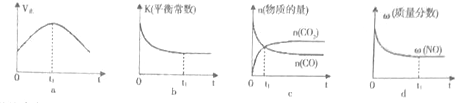
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是bd.
(4)汽车尾气中NOx和CO的生成及转化.
①已知汽缸中生成NO的反应为N2(g)+O2(g)?2NO(g)△H>0,汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是温度升高,平衡正向移动,NO的含量增大.
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)═2C(s)+O2(g)△H>0,判断该设想能否实现:不能(填“能”或“不能”),简述其依据:;△H>0△S<0,则在任何温度下△G>0,不可能自发进行.
(1)将PM2.5样本用蒸馏水处理制成待测试样,测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离 子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2)洗涤含SO2的烟气,下列物质可作洗涤剂的是bc
a.CaCl2 溶液 b.Na2CO3 溶液 c.Ca(OH)2 悬浊液 d.浓H2SO4
(3)安装汽车尾气催化转化器也可减轻PM2.5的危害,其反应是:
2NO(g)+2CO(g)$\frac{\underline{\;催化剂\;}}{\;}$2CO2(g)+N2(g);△H<0
①该反应平衡常数表达式K=$\frac{{c}^{2}(C{O}_{2})c({N}_{2})}{{c}^{2}(NO){c}^{2}(CO)}$;温度升高K值减小(填“增大”或“减小”)
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是bd.

(4)汽车尾气中NOx和CO的生成及转化.
①已知汽缸中生成NO的反应为N2(g)+O2(g)?2NO(g)△H>0,汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是温度升高,平衡正向移动,NO的含量增大.
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)═2C(s)+O2(g)△H>0,判断该设想能否实现:不能(填“能”或“不能”),简述其依据:;△H>0△S<0,则在任何温度下△G>0,不可能自发进行.
6.下列有关反应的颜色变化中,不正确的是( )
| A. | 盐酸能使酚酞试液变红 | B. | 氯水久置后黄绿色消失 | ||
| C. | SO2使品红溶液褪色 | D. | 淀粉溶液遇碘单质变蓝 |
5.下列实验误差分析错误的是( )
| A. | 用湿润的pH试纸测稀碱液的pH,测定值偏小 | |
| B. | 滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小 | |
| C. | 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 | |
| D. | 测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏小 |
3.已知A、B、C、D、E五种元素都是元素周期表中前20号元素,原子序数依次增大,E的特征电子排布式为4s2.A、B、C、D四种元素在元素周期表中的相对位置如下表所示.
根据以上信息,下列叙述不正确的是( )
| … | A | ||||||
| B | C | D |
| A. | 元素C在元素周期表d区 | |
| B. | D的电子排布式为1s22s22p63s23p5 | |
| C. | A氢化物沸点高于D的氢化物沸点 | |
| D. | A和B的离子中,半径较小的是B的离子 |
2.下列叙述正确的是( )
| A. | 某元素基态原最外层有3个未成对电子,最内层有2个电子,其元素符号为N | |
| B. | 某元素的负一价离子的电子层结构与氩相同,其基态原子价电子排布式为[Ne]3s23p5 | |
| C. | 某元素的正三价离子的3d能级为半充满,其基态原子排布式为[Ar]3d64s2 | |
| D. | 某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的电子排布式为[Ar]3d54s1 |
20.在NH3、H2SO4的工业生产中,具有的共同点是( )
0 170256 170264 170270 170274 170280 170282 170286 170292 170294 170300 170306 170310 170312 170316 170322 170324 170330 170334 170336 170340 170342 170346 170348 170350 170351 170352 170354 170355 170356 170358 170360 170364 170366 170370 170372 170376 170382 170384 170390 170394 170396 170400 170406 170412 170414 170420 170424 170426 170432 170436 170442 170450 203614
| A. | 使用催化剂 | B. | 使用尾气吸收装置 | ||
| C. | 使用H2作原料 | D. | 使用吸收塔设备 |




 .
.