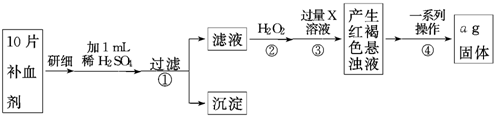
5.设阿伏加德罗常数的数值为NA,下列说法正确的是( )
| A. | 1 mol S与足量Fe反应,转移的电子数为3NA个 | |
| B. | 1.5 mol NO2与足量H2O反应,转移的电子数为2NA个 | |
| C. | 常温常压下,46 g的NO2和N2O4混合气体含有的原子数为3NA个 | |
| D. | 100 ml 0.10mol/L的氨水中,含NH3•H2O 分子0.01NA个 |
4.下列物质既能够与强酸又能够与强碱反应,且反应后都能产生气体的是( )
| A. | 硫化铵 | B. | 亚硫酸氢钾 | C. | 碳酸氢钠 | D. | 硫酸氢铵 |
3.电解稀H2SO4、CuCl2的混合液,最初一段时间阴极和阳极上分别析出的物质分别是( )
| A. | H2和Cl2 | B. | Cu和 Cl2 | C. | H2和O2 | D. | Cu和O2 |
2.下列电离方程式错误的是( )
| A. | NH3•H2O?NH4++OH- | B. | H2SO3?2H++SO32- | ||
| C. | Fe(OH)3?Fe3++3OH- | D. | H2SO4→2H++SO42- |
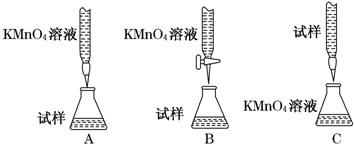
20.下列实验所选装置不合适的是( )

| A. | 分离水和泥沙选① | B. | 从盐水中获得食盐选② | ||
| C. | 分离酒精和水选③ | D. | 由自来水制取纯净水选④ |
19.用如图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应.下列实验不合理的是( )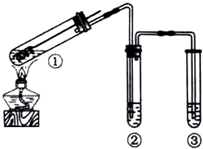

| A. | 为确认CuSO4生成,向①中加水,观察颜色 | |
| B. | 上下移动①中铜丝可控制SO2的量 | |
| C. | ②中选用品红溶液验证SO2的生成 | |
| D. | ③中选用NaOH溶液吸收多余的SO2 |
18.(CN)2、(SCN)2等的性质与卤素单质相似,在化学上称为“类卤素”;CN-、SCN-等的性质也与卤离子相似,称为“类卤离子”;不同卤原子能组成卤素互化物,如溴化碘IBr,下面叙述正确的是( )
| A. | (CN)2在碱溶液中生成CN-和OCN- | |
| B. | IBr+2NaOH═NaBr+NaIO+H2O | |
| C. | 均能在空气中燃烧 | |
| D. | IBr与苯发生取代反应生成溴苯和碘化氢 |
17.下列物质中,不能用直接化合制取的是( )
| A. | Fe(OH)3 | B. | FeCl3 | C. | CuS | D. | FeCl2 |
16.下列离子方程式书写正确的是( )
0 169848 169856 169862 169866 169872 169874 169878 169884 169886 169892 169898 169902 169904 169908 169914 169916 169922 169926 169928 169932 169934 169938 169940 169942 169943 169944 169946 169947 169948 169950 169952 169956 169958 169962 169964 169968 169974 169976 169982 169986 169988 169992 169998 170004 170006 170012 170016 170018 170024 170028 170034 170042 203614
| A. | 苯酚与碳酸钠反应:2C6H5OH+CO32-→2C6H5O-+CO2↑+H2O | |
| B. | 用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ | |
| C. | Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-═2Fe2++I2+3H2O | |
| D. | SO2通入溴水中:SO2+2H2O+Br2═2H++SO42-+2HBr |