16.在NaCl、MgCl2两种盐配制的混合液中,Na+为0.2mol,Mg2+为0.25mol,则Cl-为( )
| A. | 0.5 mol | B. | 0.6 mol | C. | 0.7 mol | D. | 0.8 mol |
15.取某铁的氧化物样品,用140mL 5mol/L盐酸恰好使其完全溶解,所得溶液还能吸收标准状况下0.56L氯气,使其中的Fe2+ 完全转化为 Fe3+,该样品中可能的化学式是( )
| A. | Fe3O4 | B. | Fe4O5 | C. | Fe5O6 | D. | Fe5O7 |
14.关于下列四个图象的说法中正确的是( )


| A. | 图①表示可逆反应CO(g)+H2O(g)?CO2(g)+H2(g)中的△H大于0 | |
| B. | 图②是石墨为电极电解氯化钠稀溶液,阴、阳两极产生气体体积之比一定为1:1 | |
| C. | 图③表示25℃,0.1 mol•L-1盐酸滴定20 mL 0.1 mol•L-1 NaOH溶液,pH随加入酸体积的变化 | |
| D. | 图④表示2SO2(g)+O2(g)?2SO3(g)△H<0 正、逆反应平衡常数K随温度的变化 |
13.下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是Ar,只有负价而无正价的元素是F,可用于制半导体材料的元素是Si
(2)C元素在元素周期表中的位置是三周期ⅢA族.
(3)最高价氧化物的水化物碱性最强的是NaOH,酸性最强的是HClO4,呈两性的是Al(OH)3;
(4)A分别与E、G、H形成的化合物中,最稳定的HF;
(5)在B、C、E、F中,原子半径最大的是Na.
(6)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式Al(OH)3+NaOH=NaAlO2+2H2O.
(7)B、H两种元素形成的化合物所含的化学键类型为离子键
(8)写出C的最高价氧化物与H的氢化物之间反应的离子方程式Al2O3++6H+=2Al3++3H2O.
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | |||||
| 3 | B | C | J | F | H | I |
(2)C元素在元素周期表中的位置是三周期ⅢA族.
(3)最高价氧化物的水化物碱性最强的是NaOH,酸性最强的是HClO4,呈两性的是Al(OH)3;
(4)A分别与E、G、H形成的化合物中,最稳定的HF;
(5)在B、C、E、F中,原子半径最大的是Na.
(6)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式Al(OH)3+NaOH=NaAlO2+2H2O.
(7)B、H两种元素形成的化合物所含的化学键类型为离子键
(8)写出C的最高价氧化物与H的氢化物之间反应的离子方程式Al2O3++6H+=2Al3++3H2O.
12.元素R的质量数为A,Rn-的核外电子数为x,则ngRn-所含中子的物质的量为( )
| A. | (A-x+n)mol | B. | (A-x-n)mol | C. | (A-x+n)n/Amol | D. | (A-x-n)n/Amol |
11.在相同温度下,下列3个反应放出的热量分别以Q1、Q2、Q3表示,则Q1、Q2、Q3的关系是( )
(1)2H2(气)+O2(气)═2H2O(气)+Q1
(2)2H2(气)+O2(气)═2H2O(液)+Q2
(3)H2(气)+O2(气)═H2O(气)+Q3.
(1)2H2(气)+O2(气)═2H2O(气)+Q1
(2)2H2(气)+O2(气)═2H2O(液)+Q2
(3)H2(气)+O2(气)═H2O(气)+Q3.
| A. | Q1>Q2,Q2=2Q3 | B. | Q1=Q2=Q3 | C. | Q1<Q2,Q3=$\frac{{Q}_{1}}{2}$ | D. | 无法比较 |
10.能正确表示下列反应的离子方程式为( )
| A. | 向Fe(NO3)2稀溶液中加入稀盐酸:Fe2++2H++NO3-═Fe3++NO2↑+H2O | |
| B. | 向NaHSO4溶液中加入过量的Ba(OH)2溶液:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| C. | 向(NH4)2Mg(SO4)2溶液中加入少量的Na2O:Mg2++Na2O+H2O═Mg(OH)2↓+2Na+ | |
| D. | 向0.1mol•L-1、pH=1的NaHA溶液中加入NaOH溶液:HA-+OH-═A2-+H2O |
9.维生素C的结构简式如图,有关它的叙述错误的是( )
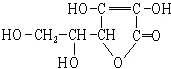

| A. | 分子式为C6H8O6 | B. | 易起氧化及加成反应 | ||
| C. | 可以溶于水 | D. | 在碱性溶液中能稳定地存在 |
8.下列说法错误的是( )
| A. | 2p | B. | 3f | C. | 4p | D. | 5s |
7.根据键能数据:H-Cl 431kJ/mol,H-I 299kJ/mol,由此可得出的结论是( )
0 169545 169553 169559 169563 169569 169571 169575 169581 169583 169589 169595 169599 169601 169605 169611 169613 169619 169623 169625 169629 169631 169635 169637 169639 169640 169641 169643 169644 169645 169647 169649 169653 169655 169659 169661 169665 169671 169673 169679 169683 169685 169689 169695 169701 169703 169709 169713 169715 169721 169725 169731 169739 203614
| A. | 溶于水时,HI分子比HCl分子更容易电离 | |
| B. | HI比HCl熔、沸点都高 | |
| C. | HI比HCl更稳定 | |
| D. | 拆开相同物质的量的HI分子比HCl消耗的能量小,HI是离子化合物 |